2010年07月02日
ヒルジン:抗トロンビン薬(2)
抗血栓療法:抗トロンビン薬(1)より続く
【ヒルジン】
自然界には抗凝固活性を示す物質がいくつか知られていますが、その一つとしてヒルの唾液腺分泌物に含まれる抗凝固物質があります。医療用ヒル(Hirudo medicinalis)は、1世紀以上も前より静脈性うっ血状態に使用されてきた歴史があります。1884年、Haycraftはこの抗凝固物質について初めて報告し、1904年、Jacobyによってヒルジンと命名されました。
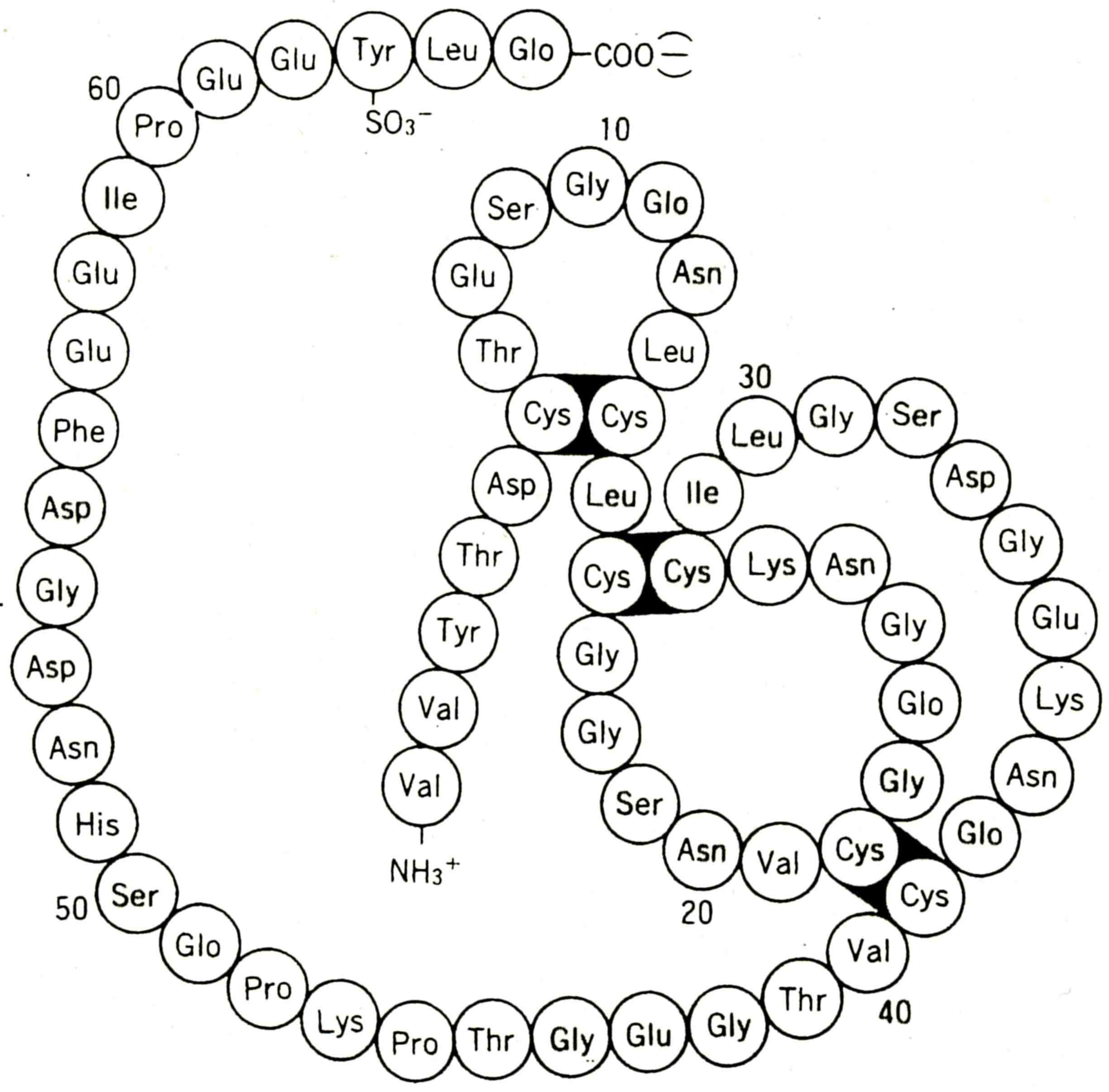
天然ヒルジンは65個のアミノ酸からなる分子量約7,000のポリペプチドです(上図)。
トロンビンと1:1複合体を形成することにより抗凝固活性を発輝します。
ヘパリン類との相違点としては、
(1)アンチトロンビン(AT)非依存性にトロンビン活性を阻止すること
(2)フィブリンに吸着されているトロンビンに対しても強い阻止効果を発輝すること
(3)血漿中蛋白と結合しないため血小板第4因子(PF4)により中和されることはないこと
(4)ヘパリン起因性血小板減少症(heparin induced thrombocytopenia: HIT)発症の懸念がないこと
などが挙げられています。血栓性疾患においては、しばしばヘパリン結合血漿蛋白が上昇するため、このことが未分画ヘパリンの効果の個人差(無効例の存在)の一因と考えられてきましたが、ヒルジンではこの懸念がありません。
ヒルジンの臨床応用を可能にしたのは、遺伝子工学的手法によるヒルジンの大量生産によるところが大きいです。実用化には至りませんでしたが、本邦でも播種性血管内凝固症候群(DIC)治療薬として臨床試験が行われた歴史があります。
現在、天然性ヒルジンの部分的なアミノ酸残基の置換や、N末端領域の修飾を行ったいくつかの遺伝子組換え型ヒルジンが知られています。遺伝子組み換えヒルジンは、天然ヒルジン同様に65個のアミノ酸残基よりなり、6-14、16-28、22-39の3ケ所にジスルフィド結合(S-S結合)を形成しています。desirudinは欧州にて、lepirudinは米国にて使用可能です。
ヒルジンのC末端は、トロンビンの陰イオン結合部位とイオン結合し、ヒルジンのN末端側はトロンビンの無極性部位と結合することにより、ヒルジンはトロンビンと高度の親和性を有し複合体を形成すると考えられています。この結果、トロンビンによる全ての向凝固作用が消失し、凝固活性化のpositive feedbackが抑制されるものと考えられます。
また、ヒルジンと結合したトロンビンはATと結合できないため、ATの消費を抑制する効果も期待されています。なお、トロンビンとフィブリノゲンとの親和性よりも、トロンビンと血小板膜表面上のトロンビン受容体との親和性が高度であるため、凝固を阻止するヒルジン濃度は血小板活性化を阻止しないものと考えられています。
トロンビンはフィブリノゲンをフィブリンに転換することで向凝固作用を有しますが、この際、トロンビンはフィブリンへの結合能も有しています。このことは、生じたトロンビンをフィブリン内に埋没させることにより、トロンビンの効果を消失させるnegative feedbackとしての意義を有しています。
しかし、このようにフィブリンに結合したトロンビンは依然として凝固活性を有しており、線溶療法時に血栓が溶解しフィブリンに結合したトロンビンが再露呈されることが線溶療法後の再閉塞の一因と考えられています。
このフィブリン結合トロンビンは、ヘパリン・アンチトロンビン複合体では阻止されにくいですが、ヒルジンはフィブリン結合トロンビンをも有効に阻止することが可能です。
ヒルジンの血中半減期は0.6〜2時間と報告されており、大部分が腎で代謝されます。そのため腎不全合併症例においてはクリアランスが著しく遅延し、投与量の注意が必要です(腎不全合併症例における検討では、血中半減期は15〜41hrと延長しています)。
(続く)
bivalirudin (Hirulog、ヒルログ):抗トロンビン薬(3)へ
【リンク】
投稿者:血液内科・呼吸器内科at 01:26| 抗凝固療法