ヘパリン在宅自己注射療法(インデックス)
<ヘパリン在宅自己注射療法>インデックス
1)抗リン脂質抗体症候群に対するヘパリン皮下注
<リンク>
<ヘパリン在宅自己注射療法の適応と指針>
ヘパリン在宅自己注射療法(インデックス)
平成23年9月に日本産科婦人科学会、日本産婦人科医会、日本産婦人科・新生児血液学会、日本血栓止血学会の4学会が「ヘパリン在宅自己注射療法の適応と指針」を厚生労働省に提出し、平成 24 年 1 月にヘパリン在宅自己注射が保険収載された経緯があります。
ヘパリン在宅自己注射療法の適応と指針.公益社団法人日本産科婦人科学会,公益社団法人日本産婦人科医 会,日本産婦人科・新生児血液学会,一般社団法人日本血栓止血学会,2011. http://www.jsognh.jp/common/files/society/demanding_paper_07.pdf
一部のみ、こちらで抜粋して紹介したいと思います。
正式には、必ず上記サイトをご覧いただきたいと思います。
ヘパリン在宅自己注射療法の適応と指針(上記サイトより一部のみ抜粋)
目的および意義
ヘパリン在宅自己注射の目的は、通院の際に生じる身体的、時間的、経済的負担を軽減させ、患者により質の高い社会生活を送らせることである。
特に対象となる妊婦や血栓性素因を持つ患者にとって、毎日朝夕2回の通院は大きな負担となっており、ヘパリン在宅自己注射が是非とも必要である。
適応基準(以下の(1)〜(6)すべてを満足していること)
(1)ヘパリンに対してのアレルギーがなく、HITの既往がないこと。
(2)他の代替療法に優る効果が期待できるヘパリン治療の適応患者であること。
(3)在宅自己注射により通院の身体的、時間的、経済的負担、さらに精神的苦痛が軽減され、生活の質が高められること。
(4)以下の1)〜3)のいずれかを満足し、担当医師が治療対象と認めた患者
1)血栓性素因(先天性アンチトロンビン欠乏症、プロテインC欠乏症、プロテインS欠乏症、APSなど)を有する患者
2)深部静脈血栓症、肺血栓塞栓症既往のある患者
3)巨大血管腫、川崎病や心臓人工弁置換術後などの患者
(5)患者ならびに家族(特に未成年者の場合)が、目的、意義、遵守事項などを十分に理解し、希望していること。
(6)医師、医療スタッフとの間に安定した信頼関係が築かれていること。
患者教育:省略
患者の遵守事項:省略
方法
(1)皮下注射用ヘパリンを1回につき5,000単位、12時間ごと(1万単位/日)に皮下に自己注射する。
(2)注射部位は、腹部、大腿、上腕とする。
認可(自己注射療法開始条件):省略
管理と記録:省略
ヘパリン在宅自己注射療法(インデックス)
<慢性DICに対するヘパリン皮下注>
ヘパリン在宅自己注射療法(インデックス)
大動脈瘤、巨大血管腫、緩徐に進行する癌などで慢性DICを合併した場合に、DICの合併のために退院できない場合があります。
そのような場合に、ヘパリン在宅自己注射は優れた治療選択肢となります。
DICにおいては基質としての凝固因子を低下させてもDICの本態である凝固活性化を抑制することができませんが、活性型凝固因子(トロンビンや活性型第X因子など)を抑制して初めてコントロールが可能です。
実際、DICに対してワルファリン(基質としてのビタミンK依存性凝固因子を低下させる薬剤)を投与すると無効であるばかりでなく、大出血の合併症がみられることがあり、禁忌です。
また、劇症肝炎は凝固因子が枯渇する病態ですがやはりDICを発症します。
活性型凝固因子を阻止する薬剤としては、ヘパリン類が知られています。
在宅で治療する場合には通常ヘパリン5000単位を1日2回皮下注します。
ただし、低体重、腎障害合併例では減量して用います。
大動脈瘤、巨大血管腫では線溶亢進型DICを合併することが特徴的であり、臓器障害よりも出血症状が見られやすいです(ただし、動脈瘤などではDICではなく基礎疾患に起因する腎障害をきたすことがあります)。
ヘパリン在宅自己注射を導入する場合には、必ず入院の上、出血の副作用がみられないかチェックする必要があります。
なお、線溶亢進型DICの典型例ではヘパリンのみではなくトラネキサム酸(商品名:トランサミン)を併用した方が出血症状に対して有効な場合がありますが、トラネキサム酸は致命的な血栓症を誘発することもあるため、必ず専門家にコンサルトすべきです。
前述のように、DICに対してワルファリンは禁忌ですが、新規経口抗凝固薬(NOAC)はトロンビンまたは活性型第X因子を直接抑制するためにDICに対して有効である可能性があります。
保険適応がないため現時点では使用できませんが、検討の価値があります。
朝倉英策. 新規経口抗凝固薬(NOAC). 朝倉英策・編. 臨床に直結する血栓止血学. 東京:中外医学社; 2013. pp.321-329.
Hayashi T, et al.: Rivaroxaban in a Patient with Disseminated Intravascular Coagulation Associated with an Aortic Aneurysm. Ann Intern Med, 15: 158-159, 2014.
ヘパリン在宅自己注射療法(インデックス)
<抗リン脂質抗体症候群に対するヘパリン皮下注>
ヘパリン在宅自己注射療法(インデックス)
抗リン脂質抗体症候群(APS)は、動・静脈血栓症または不育症(習慣性流産を含む)といった臨床症状がみられ、かつ、抗カルジオリピン抗体(特にβ2GPI依存性のもの)またはループスアンチコアグラントのうち1項目以上が陽性の場合に診断される、最も高頻度にみられる後天性血栓性素因です。
本疾患に対しては、ワルファリンによる抗凝固療法が血栓症発症の二次予防に有効と報告されていますが、ワルファリンには催奇性の副作用があるため挙児希望の若年女性に対しては使用できません。
在宅環境であるにもかかわらず、抗凝固療法として本来は簡便である経口薬ワルファリンを使用できない(ヘパリン皮下注を行わざるを得ない)理由としては、挙児希望の女性におけるワルファリンの催奇形性の問題が大きいです。
この点、ヘパリン在宅自己注射(皮下注)は、挙児希望のAPS女性に対して最も大きい意義を有しています。
APSにおける不育症の機序はいくつか報告されていますが、胎盤内における血栓形成は大きな機序の一つであり、抗血栓療法は理にかなった治療です。
APSにおける不育症(習慣性流産を含む)対策としては、低用量アスピリン(経口)&ヘパリン(皮下注)併用療法が標準的治療として確立されています。
当科では、APSの診断がなされた場合には挙児希望があった時点よりアスピリン(100mg/日)の内服を開始し、妊娠成立時点でヘパリン(5000単位を12時間ごとに皮下注)の自己注射を開始しています。
アスピリンは妊娠36週まで内服し(出産1週間前まで投与することもあります)、ヘパリン皮下注は分娩前日までの投与を原則としていますが、よりリスクが高い症例では分娩前よりへパリン持続点滴に切り替え、分娩4〜6時間前に中止する方法をとっています。
アスピリン&ヘパリン併用療法以外にも、アスピリン単独投与の有用性の報告もあります。
実際、APSの病勢が低いと考えられる症例などでアスピリン単独療法が行われることも多いと思われます。
アスピリンは胎盤を通過し、その血小板機能抑制作用は約1週間持続します。
胎児における動脈管早期閉鎖などの先天異常の可能性については欧米の報告で否定されていますが、内服時期によっては分娩時の出血量の増加につながるとの報告もあります。
本邦では、添付文書上、「出産予定日12週以内の妊婦には投与しないこと」と記載されており、アスピリン投与についてはその投与期間についても十分な説明と同意が必要です。
2012年よりヘパリンカルシウムの在宅自己注射が保険適用となり、APS合併妊婦を取り巻く医療環境は医療費および保障の面でも大きく前進しました。
ただし、長期にわたるヘパリン皮下投与は精神的にも手技的にも患者負担の大きい治療であることに変わりはないです。
医師による指導のみならず、産科医療に携わるすべてのスタッフの理解と協力が必要と考えられます。
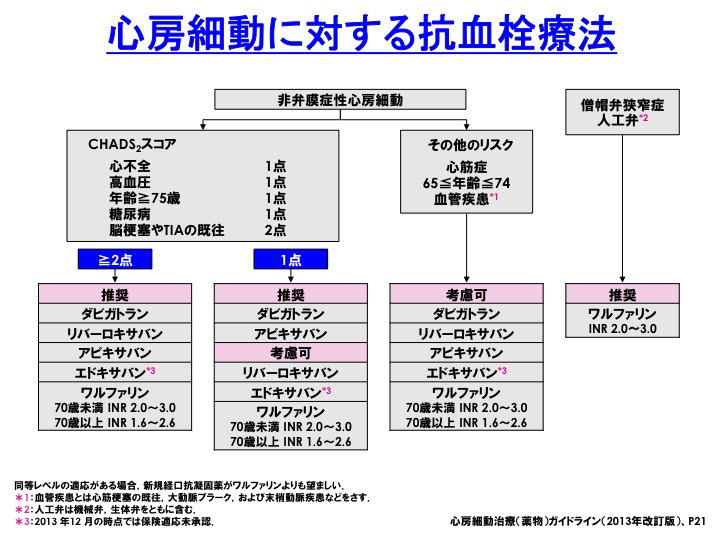
このガイドライン作成時には、リバーロキサバンやエドキサバンは、CHADS2スコアが1点のエビデンスがなかったために考慮可に留まっていますが、管理人はその他のNOACとあまり変わらないのではと理解しています。
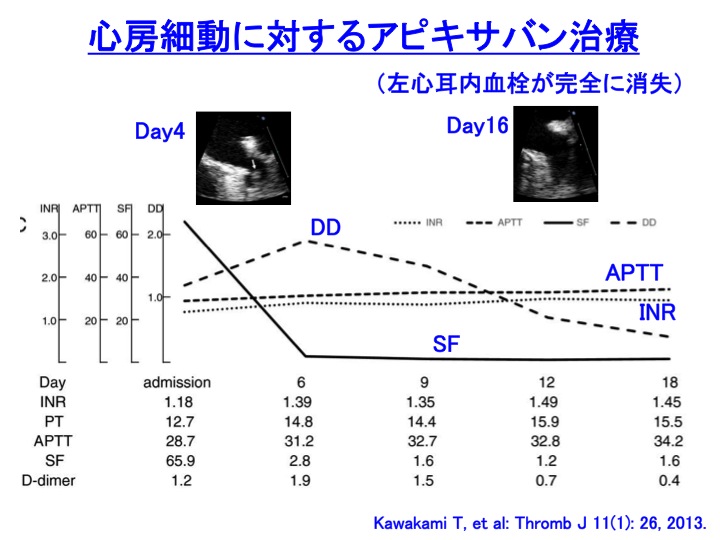

抗凝固療法を開始する前には、DICの合併の有無をチェックするために、一度はフィブリノゲンやFDP(D-ダイマー)をみておきたいところです。
DICの合併があれば、出血に対する注意がさらに大切になってきます。
いずれのマーカーも1回のみの測定ではなく、定期的にチェックしたいところです。
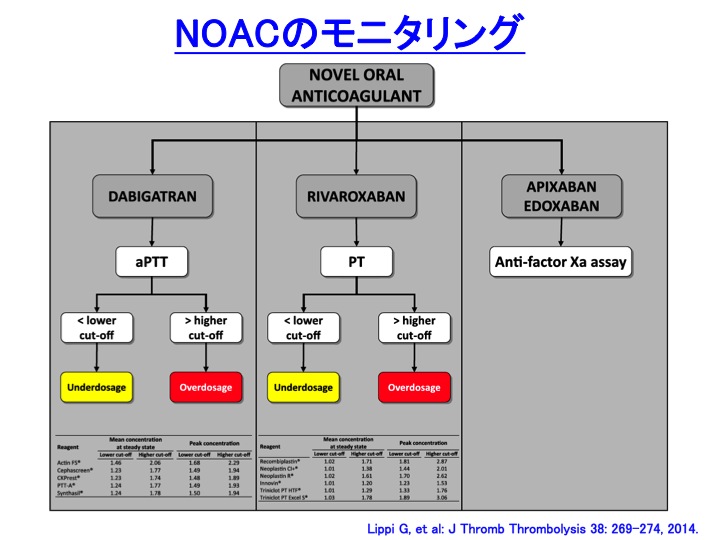
新規経口抗凝固薬のモニタリングでは、測定周期をどうするかはいろんな意見があると思いますが、3〜4ヶ月くらいの周期でしょうか(ワルファリンのように毎回は必要ないと思います)。


<リンク>推薦書籍「臨床に直結する血栓止血学」
<リンク>推薦書籍「臨床に直結する血栓止血学」
<リンク>推薦書籍「臨床に直結する血栓止血学」
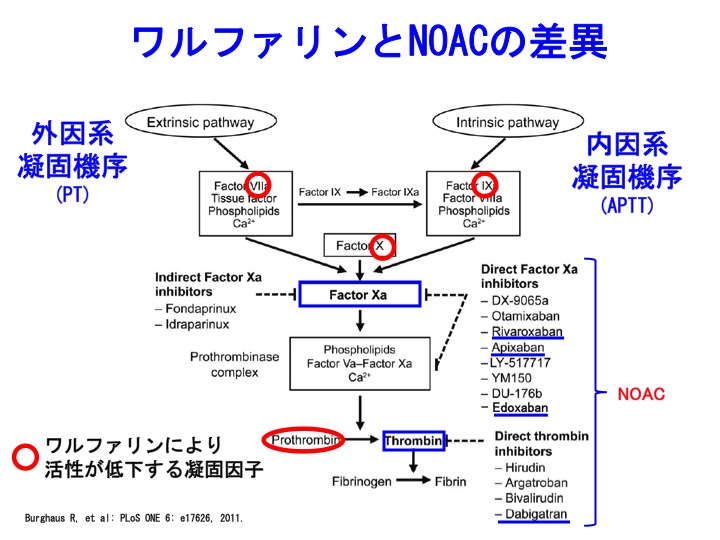

経口可能な抗凝固薬としては、長年にわたりワルファリンのみが用いられてきました。
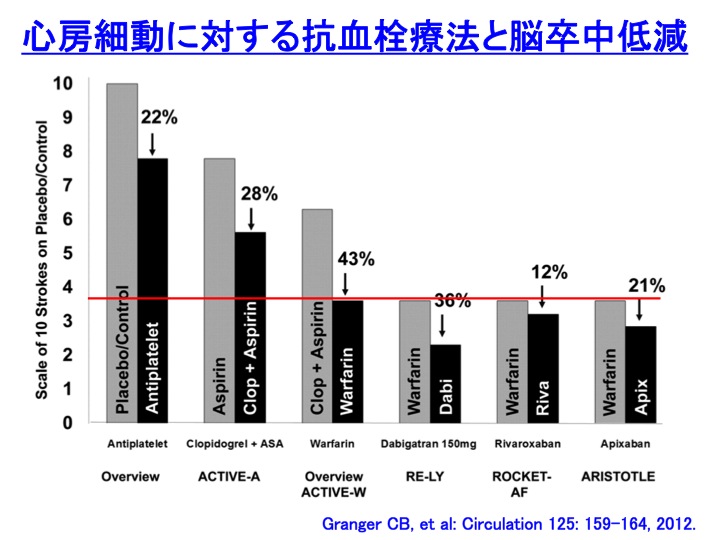
近年、ダビガトラン(商品名:プラザキサ)、リバーロキサバン(商品名:イグザレルト)、エドキサバン(商品名:リクシアナ)、アピキサバン(商品名:エリキュース)といった新規経口抗凝固薬が続々と登場して、ワルファリンに代わる画期的な経口抗凝固薬として、大変に期待されています。
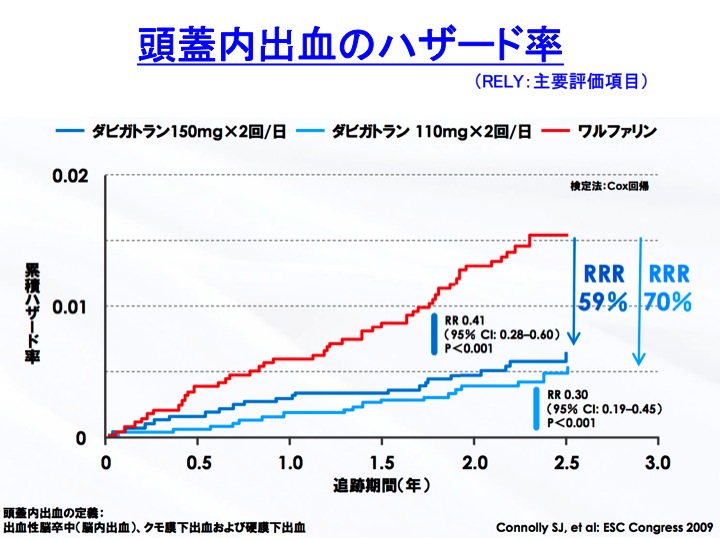
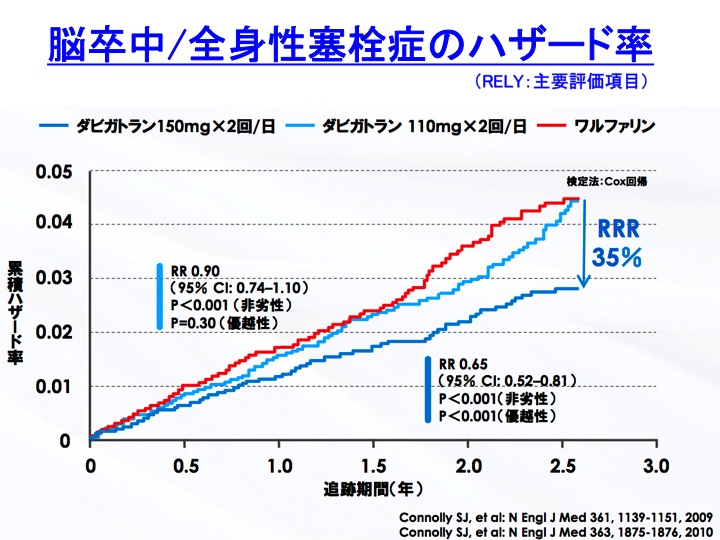
大規模臨床試験の結果から、これらの薬物はワルファリンより効果の点で同等以上であり、副作用(特に頭蓋内出血)も少ない点で期待が寄せられました。
また、ワルファリンのように頻回の採血によるモニタリングが必要ない点が最初のころはキャッチフレーズとなりました(ただし、後述のようにやはりモニタリングは重要と考えられます)。
当初、new oral anti-coagulant(略称:NOAC)と言われていましたが、いつまでもnewというのは違和感がありますので、novel oral anti-coagulant、non-VKA oral anti-coagulantとも言われています。いずれも、NOACになります。
NOACの通りが良いので、NOACの略称になるように、newを変えていったという要素もあるかも知れません。
あるいは、アンチトロンビン非依存性に活性型凝固因子を抑制しますので、direct oral anti-coaglant(DOAC)という表現の仕方もあります。
これらの新規経口抗凝固薬は、循環器領域、脳卒中領域、血栓止血・血液内科領域、血管外科/内科領域、臨床検査医学領域などいろんな領域で話題になっています。
これらの薬物が大きく育つためにも、モニタリングの意義も大きいのではないかと考えられます。
がん患者と抗血栓療法(抗凝固/血小板療法)(インデックス)
<インデックス>
1)血栓症の分類
2)治療の考え方
3)アスピリン
4)ワルファリン
5)モニタリング
<リンク>推薦書籍「臨床に直結する血栓止血学」
がん患者と抗血栓療法(抗凝固/血小板療法)(5)
<抗凝固療法のモニタリング>
抗凝固薬のうち経口薬であるワルファリン、注射薬であるヘパリンともにモニタリングを適切に行うことで安全かつ効果的な治療を継続できます。
その際、効果、安全性の両面からの評価は肝要です。
新規経口抗凝固薬はまだ定まったモニタリング法はないため、表では私案として記載しました。
| 薬 剤 | 効 果 | 副作用(出血) |
| 未分画へパリン | FDP、Dダイマー、TAT、SFなど | APTT(通常1.5〜2.0倍)(※1) |
| 低分子へパリン | FDP、Dダイマー、TAT、SFなど | APTT(常用量では延長しない) |
| ダナパロイド | FDP、Dダイマー、TAT、SFなど | APTT(常用量では延長しない) |
| ワルファリン | F1+2、Dダイマー、TAT、SFなど | PT-INR(通常2.0〜3.0)(※1) |
| 新規経口抗凝固薬 | F1+2、Dダイマー、TAT、SFなど | PT、APTT(※2) |
| アスピリン(※3) |
な し | な し |
TAT:thrombin-antithrombin complex(トロンビン-アンチトロンビン複合体)
SF:soluble fibrin(可溶性フィブリン)
F1+2:prothrombin fragment 1+2(プロトロンビンフラグメント1+2)
(※1)
APTTが1.5〜2.0倍に延長していても効果を発揮しているとはかぎらない。
APTTが過度に延長している場合には出血のリスクがあると考えるべきである。
APTTが1.5〜2.0倍の状態でかつ効果判断のマーカーをチェックしたい。
PT-INRについても同様に判断する。
(※2)
新規経口抗凝固薬(NOAC):
ダビガトランはAPTTの方が延長しやすい。
イグザレルト、エドキサバンはPTの方が延長しやすい。
アピキサバンはいずれも延長しにくい。
ただし、用いる試薬によって感受性が大きく異なるため注意を要する。
いずれのNOACともに内服2〜3時間後に血中濃度がピークとなるが、そのポイントでのPT、APTTの延長が想定範囲内であることを確認する。
万一、トラフでのPT、APTTが明らかに延長していれば出血のリスクがある。
(※3)
アスピリンなどの抗血小板薬のモニタリングは研究室レベルではいくつか試みられているが、臨床の場で簡便にチェックできるマーカーはない。
<リンク>推薦書籍「臨床に直結する血栓止血学」
がん患者と抗血栓療法(抗凝固/血小板療法)(4)
<がん患者におけるワルファリン治療>
がん患者でワルファリン(ビタミンK(VK)拮抗薬)治療が行われているのは、深部静脈血栓症(DVT)や肺塞栓(PE)といった静脈血栓塞栓症(VTE)や心房細動などに罹患していたためにがん発症以前よりワルファリンを内服していた場合と、がんという血栓症の危険因子を発症したためにがん診断時または治療経過中にVTEを発症した場合があります。
いずれの場合であっても、がん化学療法とワルファリン治療が併行して行われている場合には次のような注意点があります。
1) 抗がん剤のなかには、ワルファリンの効果に影響を与えるものが少なくないため、その都度薬物相互作用の確認が必要です。
2) 抗がん剤治療に伴って食欲低下をきたすとVKの摂取も低下するため、ワルファリン過剰投与になります。
3) 抗がん剤治療により白血球数低下をきたし感染症を併発し抗生剤が投与されると、VK産生源である腸内細菌も死滅するため、ワルファリン過剰投与になります(NSAIDの併用があればさらに影響が大きいです)。
4) 肝胆膵悪性疾患(腫瘍)に伴う胆道閉塞やPTCD(経皮経肝胆管ドレナージ)のために胆汁排泄の低下をきたすと、ワルファリン過剰投与になります(VKは脂溶性ビタミンのために吸収のために胆汁が必要です)。
PT-INRを通常よりも頻回にチェックしてワルファリン用量を調整する必要があります。
化学療法に伴い食事摂取量が極端に低下することが予想される場合には、あらかじめ1週間程度ワルファリン用量を減量した上でPT-INRを追跡するのも一法です。
あるいは、入院中はヘパリンの皮下注または半減期の長いヘパリン類であるダナパロイドなどの注射薬で抗凝固療法を行い、外来移行の計画が決まった時点で退院2週間くらいまえからワルファリンへ移行するのも良いでしょう。
また、がん患者ではワルファリンの効果が不十分になりやすいことが知られているために、ワルファリンコントロール不良の如何にかかわらず入院中はヘパリン類でコントロールするという考え方もあります。
Prandoni P, et al. Recurrent venous thromboembolism and bleeding complications during anticoagulant treatment in patients with cancer and venous thrombosis. Blood. 2002; 100: 3484-88.
Akl EA, et al. Anticoagulation for the long-term treatment of venous thromboembolism in patients with cancer. Cochrane Database Syst Rev. 2014; 7: CD006650.
<リンク>推薦書籍「臨床に直結する血栓止血学」
がん患者と抗血栓療法(抗凝固/血小板療法)(3)
<がん患者における抗血小板療法>
虚血性心疾患や脳梗塞などに対してアスピリンなどの抗血小板薬内服中のがん患者において問題になるのは、化学療法や放射線療法に伴い血小板数が低下した場合に、抗血小板薬を継続できるかどうかの判断です。
この問題点を解決するエビデンスとなるような臨床試験は存在しませんが、通常血小板数が3〜5万/μL以上であれば、抗血小板療法を継続できる場合が多いです。
一方、血小板数が3〜5万/μL未満となった場合には、抗血小板療法を継続することのメリット(動脈血栓症の予防)とデメリット(出血の副作用)を比較して慎重に判断することになります。
なお、一般的には、血栓症では致命的になることが少なくないですが、出血の副作用で致命症になるのは例外的です。
判断に迷った場合には、血栓症対策に比重をおく方が良い場合が多いです。
<リンク>推薦書籍「臨床に直結する血栓止血学」