先天性凝固異常症(10)まとめ
先天性凝固異常症(9)第XIII因子欠乏/異常症より続く。
先天性凝固異常症(10)まとめ
血友病やvWD以外のまれな凝固因子欠乏症に遭遇した場合、一番悩むのが補充療法です。
先天性FVII欠乏症やFXI欠乏症など、凝固活性と出血症状が相関しない場合もあり、血液製剤の投与量や投与間隔は出血の既往や重症度、出血の程度、それぞれの凝固因子の必要な止血レベル、生体内回収率・半減期などを考慮し、治療計画を立てる必要があります。
十分量の補充療法を行っても、大出血や手術時には消費により半減期が短縮することがあるため、凝固因子活性のモニタリングを施行しながら止血管理を行うべきです。
さらに、FFPの使用は2005年の血液製剤の使用指針に則って適性使用を心掛けると同時に、血漿由来血液凝固因子製剤の使用にあたっては感染症や抗体産生などの危険性を常に認識しながら使用すべきです。
参考文献
・滝正志,他.血液凝固異常症全国調査,平成23年度報告書(財団法人エイズ予防財団).2012.
・Peyvandi F, Duga S, Akhavan S, Mannucci PM. Rare coagulation deficiencies. Haemophilia. 2002; 8: 308-321.
・Mannucci PM, Duga S, Peyvandi F. Recessively inherited coagulation disorders. Blood. 2004; 104: 1243-1252.
・Peyvandi F, Bolton-Mags PHB, Baltorova A, et al. Rare bleeding disorders. Haemophilia, 2012; 18: 148-153.
・Bolton-Maggs PH, Perry DJ, Chalmers EA, et al. The rare coagulation disorders - review with guidelines for management from the United Kingdom Haemophilia Centre Doctors’ Organization. Haemophilia. 2004; 10: 593-628.
(続く)先天性凝固異常症(11)先天性欠乏/異常症の特徴と製剤へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 11:16
| 出血性疾患
先天性凝固異常症(9)第XIII因子欠乏/異常症
先天性凝固異常症(8)第XII因子欠乏/異常症より続く。
先天性凝固異常症(9)第XIII因子欠乏/異常症
第XIII因子欠乏/異常症
発症頻度は200万に1人と推定されており、現在までに200例以上の報告がみられます。
FXIIIはトランスグルタミナーゼ本体であるAサブユニット(FXIII A)と、その保護に働くBサブユニット(FXIII B)のそれぞれ2つずつからなるヘテロ4量体として血中を循環しています。
欠乏症には、FXIII A遺伝子変異に起因するFXIII A欠乏症と、FXIII B遺伝子変異により二次的FXIII A低下をきたすFXIII B欠乏症とがあります。
症状
特徴的な出血症状は、臍出血と頭蓋内出血です。
その他の出血症状としては、皮下出血、血腫などがしばしば認められ、一時的に止血しても翌日に再出血する“遷延性出血(後出血)”も特徴的です。
また、習慣性流産や創傷治癒遅延も認められます。
検査所見
通常の凝血学的スクリーニング検査であるPT、APTTは正常ですので、本症を疑うときはFXIII活性や抗原量の測定が必要です。
活性測定は合成基質法、モノダンシルカダベリン法、抗原量測定はラテックス凝集法、ELISA法を用いて行います。
Aサブユニットが正常の5%以下、Bサブユニットが約半分であればFXIII A欠乏、両サブユニット共に5%以下であればFXIII B欠乏を疑います。
治療
補充療法には、血漿由来FXIII濃縮製剤が用いられます。
FXIIIの生体内回収率は100%、半減期は10日と長いため、消費機転が働かない場合は輸注されたFXIIIは長時間維持されます。
通常、FXIIIの止血レベルは2〜5%で、1回の輸注によって止血が得られます。
小出血ではFXIIIレベルを10%に、筋肉内出血では20-30%に保ちます。
しかしながら、頭蓋内出血などの重篤な出血や大手術時には創部でのFXIIIの消費が大きいため、100%以上にすることが望ましく、小手術時では50%以上を目安とします。
また、妊娠の維持にはFXIIIは必須であり10%以上を保つように、妊娠5〜6週頃よりFXIII濃縮製剤の定期補充(1-2V/週)を行います。
近年は重篤な出血の既往がある患者の出血予防を目的として、4週間隔で定期的予防投与が試みられています。
(続く)先天性凝固異常症(10)まとめへ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:55
| 出血性疾患
先天性凝固異常症(8)第XII因子欠乏/異常症
先天性凝固異常症(7)第XI因子欠乏/異常症より続く。
先天性凝固異常症(8)第XII因子欠乏/異常症
第XII因子欠乏/異常症
本症は常染色体劣性遺伝であり、世界各国で約300症例が報告されています。
APTTが著明に延長しますが、臨床的に出血傾向も血栓傾向も示しません。
検査所見
臨床症状がないため、術前検査などで偶然発見されます。
APTTが著明に延長しますがPTは基準範囲内です。
通常日本人は欧米人に比べて、FXII活性・抗原量が低値を示しますので、コントロール血漿は輸入製品ではなく自家製のものが望ましいです。
FXII活性が著明に低下し、クロスミキシング試験で欠損症パターンを呈した場合、先天性FXII欠乏/異常症を疑います。
F12遺伝子のエクソン1のCys46Tyr変異は、翻訳開始コドンATGから4塩基上流にある遺伝子多型で蛋白質翻訳に影響し、血漿FXII活性低下をもたらします。
日本人ではこの活性低下をきたす多型頻度が高く、血漿FXII活性が白人に比べて低下しています。
治療
本症は臨床的に出血の原因になりませんので、FXII活性が1%で大手術を施行する場合でも、治療は必要ありません。
(続く)先天性凝固異常症(9)第XIII因子欠乏/異常症へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:47
| 出血性疾患
先天性凝固異常症(7)第XI因子欠乏/異常症
先天性凝固異常症(6)第X因子欠乏/異常症より続く。
先天性凝固異常症(7)第XI因子欠乏/異常症
第XI因子欠乏/異常症
本症は血友病Cとも称されましたが、出血症状は血友病に比べて軽いです。
100万に1人の発生頻度と推定され、そのほとんどがアシュケナージ系ユダヤ人です。
アシュケナージ系ユダヤ人における頻度は極めて高く、一般人口の8%程度がヘテロ接合体のキャリアです。
日本人も報告が多く、40例以上が見出されています。
症状
自然出血は起こさず、外傷や外科的処置後の出血がほとんどで、特に線溶活性が高い口腔内や泌尿生殖器領域からの出血が特徴的です。
女性の場合は過多月経を認めます。
関節・筋肉内出血は稀です。
活性値と出血症状はまったく相関せず、FXI活性が1%未満の重症型でも無症候か術後の出血を認める程度の場合もあれば、軽症型で出血傾向を示す場合もあります。
ヘテロ接合体例は、臨床的には出血傾向を示しません。
検査所見
出血症状が軽度であり、術前検査などで偶然発見される場合が多いです。
APTTが著明に延長し、PTは基準範囲内にあります。
FXI活性は、過多月経のスクリーニング検査の項目としては、重要です。
FXI活性と抗原量の乖離を示す分子異常症は極めて稀であり、通常は活性も抗原量も同程度に低下するI型欠損症を呈します。
FXI活性は、通常ホモ接合体あるいは複合ヘテロ接合体例は15%未満、ヘテロ接合体例は25-70%を示します。
治療
本症では自然出血は稀なため、外傷後あるいは手術に際して補充療法を行います。
海外では血漿分画製剤としてFXI製剤があるが、本邦では補充療法としてFFPを投与します。
最小止血レベルは15-20%とされていますが、大手術時、または前立腺・下部尿路系、鼻・扁桃腺など線溶活性が高い部位の手術や外傷時には出血傾向が強く出現しますので、FXI活性を7日間、45%以上に維持することが推奨されています。
FXIの生体内回収率は90%、半減期は40-70時間で、FFP投与量は5-20 mg/kg/日で通常適切なFXIレベルに保つことが可能です。
(続く) 先天性凝固異常症(8)第XII因子欠乏/異常へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:36
| 出血性疾患
先天性凝固異常症(6)第X因子欠乏/異常症
先天性凝固異常症(5)第VII因子欠乏/異常症より続く。
先天性凝固異常症(6)第X因子欠乏/異常症
第X因子欠乏/異常症
本症の発症頻度は100万人に1人で、FVII欠乏症と類似した出血傾向を示します。稀に、FXとFVII、FXとFVIIIあるいはFXとFXIIの遺伝性欠損症があります。
症状
ホモ接合体あるいは複合へテロ接合体の患者は出血傾向を示しますが、その程度は活性の減少とよく相関します。
鼻出血、歯肉出血、過多月経、外傷や術後の過剰出血が多いですが、関節出血、頭蓋内出血など重篤な出血をきたす場合もあります。
活性が50%程度のヘテロ接合体ではほとんど出血を認めず、スクリーニング検査や家系内調査のときに偶然発見されることが多いです。
検査所見
一般的には、明らかな家族歴があり、PT・APTTともに延長、FX活性が低下しており、後天性FX欠損を除外できる場合、先天性FX欠乏症を疑います。
FX活性は低値を示しますが測定可能であり、FXノックアウトマウスの結果が示すようにFXの完全欠損は致死的です。
治療
異常出血時の治療や術前の出血予防投与には、FX補充療法としてFIX複合体製劑の輸注を行います。
一般的に止血に十分なFXレベルは10〜20%と考えられていますが、補充療法は重症度に応じて行うべきであり、軟部組織・粘膜・関節内出血には30%以上、重篤な出血に対しては50-100%になるように補充します。
FXの半減期は40-60時間と比較的長いので、出血症状を考慮しながら1日1回の投与により維持します。
後天性第X因子欠乏症
全身性アミロイドL鎖(AL)アミロイドーシスの患者で、後天性FX欠乏症を合併することはよく知られています。
治療としては、アミロイドーシスの積極的な化学療法により、FXレベルが回復し出血傾向が改善する場合があります。
(続く)先天性凝固異常症(7)第XI因子欠乏/異常症へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:54
| 出血性疾患
先天性凝固異常症(5)第VII因子欠乏/異常症
先天性凝固異常症(4)第V因子欠乏/異常症より続く。
先天性凝固異常症(5)第VII因子欠乏/異常症
第VII因子欠乏/異常症
本症はRBDの中で最も頻度が高く、2010年World Federation Hemophilia Annual Global Surveyの結果では全RBDの28%、本邦の平成23年度全国調査では22%を占めます。
発症頻度は地域によって異なり、日本では200万に1人、米国、オーストラリアでは50万人に1人、イギリスでは10万人に1人と推定されます。
症状
一般的に出血傾向は血友病より軽いですが、FVII活性が1%以下を呈するホモ接合体や複合へテロ接合体例で、重症血友病に類似した重篤な出血傾向を生じることがあります。
しかしながら、本症ではFVII活性と出血症状の重症度が一致しないことが知られており、FVII活性が1%以下でも無症候の場合もあります。
通常、皮膚粘膜出血(皮下出血、鼻出血、性器出血)、抜歯後出血、外傷後出血が主ですが、関節出血、消化管出血、頭蓋内出血、血尿、月経過多、分娩後異常出血なども認めます。
ヘテロ接合体例は無症候であるといわれてきましたが、最近の報告ではヘテロ接合体499例のうち19%が症候性で、主に皮膚粘膜出血を認めることが判明しました。
一方、まれに血栓症を伴う症例もあります。
検査所見
本症は、出血症状が軽度あるいは無症候であるために、術前検査などで発見されます。
PT延長を示しますが、APTTは基準範囲以内です。
FVII活性が低下し、後天性FVIIインヒビター発生や、肝機能障害、VK欠乏などが除外された場合、先天性FVII欠乏症を疑います。
FVIIaと組織因子との相互作用領域に変異がある場合は、FVII活性の測定に用いる組織因子(TF)の動物種の違いにより検査成績に乖離を示しますので、ヒトTF、ウサギTF、ウシTFの3種類を測定試薬として用います。
治療
関節内出血や頭蓋内出血などの重症出血患者、ならびにFVII活性低下・出血の既往・手術部位によって過剰出血が予測される術前患者では、FVIIを十分含む製剤による補充療法が必要となります。
現在日本で使用できる製剤には、遺伝子組換え活性型FVII製剤(rFVIIa)と血漿由来FIX複合体製劑があります。
FVII活性が10-25%あれば、止血が可能です。
rFVIIaは15〜30 mg/kg (0.75〜1.5 K IU/kg)を止血が得られるまで4〜6時間ごとに投与することで安全かつ有効に止血が図れますが、高価な薬剤です。
一方、複合型FIX濃縮製剤で補充療法を行うと、血栓症などの合併症を併発しやすいので注意が必要です。
また、FFPによる補充療法は、FVIIの半減期が4〜6時間と短く循環血液量の過剰をきたすため困難なことが多いです。
一方、無症候の患者で侵襲の少ない手術(抜歯など)の場合は、トラネキサム酸の投与が有効です。
(続く)先天性凝固異常症(6)第X因子欠乏/異常症へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:40
| 出血性疾患
先天性凝固異常症(4)第V因子欠乏/異常症
先天性凝固異常症(3)先天性プロトロンビン低下/異常症より続く。
先天性凝固異常症(4)第V因子欠乏/異常症
第V因子欠乏/異常症
本症はパラ血友病(血友病類似症)とも称され、100万人に1人の発生頻度と推定されます。
症状
ホモ接合体では、頭蓋内出血などの重症例もありますが、多くは血友病に比べて出血症状は軽く、無症候の場合もあります。
皮膚粘膜出血(歯肉出血、鼻出血)、血腫および過多月経が最も一般的な症状です。
血漿FV活性と出血症状の重症度は、必ずしも一致しません。
FVの80%は血中、20%は血小板α顆粒中に存在しますので、出血症状は血小板中のFV量も考慮する必要があります。
FV異常症は血栓傾向をきたす場合もあり、特にArg506がGlnに置換したFV Leiden変異は欧米で高率に認められる先天性血栓性素因の一つとして重要です。
日本人を含む東洋人には、FV Leidenは存在しませんが、活性化プロテインC(APC)抵抗性を示し血栓症を発症したFV異常症は本邦でも2家系認められまあす。
検査所見
PT、APTTともに延長しますが、ヘパプラスチンテストは正常です。
FV活性の低下を認め、クロスミキシング試験にて後天性FVインヒビターを否定できた場合、先天性FV欠乏/異常症を疑います。
FV Leidenは、FVの凝固活性測定値には異常を認めませんので、APC抵抗性試験を行う必要があります。
治療
外傷・抜歯・外科手術時、重症出血時などの止血管理には、FFP投与を行います。
FFP中のFVは速めに失活するため、調整後2カ月以内のFFPを使用することが重要です。
FVの生体内回収率は50〜100%、半減期は36時間です。
FFPはまず15〜20ml/kgを静注し、続いてFV活性20%を維持するように補充します。
鼻出血や歯肉出血には、トラネキサム酸が有効です。
(続く) 先天性凝固異常症(5)第VII因子欠乏/異常症へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:56
| 出血性疾患
先天性凝固異常症(3)先天性プロトロンビン低下/異常症
先天性凝固異常症(2)先天性フィブリノゲン欠乏症より続く。
先天性凝固異常症(3)先天性プロトロンビン低下/異常症
先天性プロトロンビン低下/異常症
ホモ接合体あるいは複合へテロ接合体の発症頻度は、200万人に1人と極めて稀です。
活性および抗原を完全に欠失する無プロトロンビン血症はいまだに報告がなく、致死的と考えられています。
本邦では低下症は1家系のみ、異常症はProthrombin Tokushima、Obihiro、Himi、Kawaguchiなどの報告があります。
症状
一般的にプロトロンビン低下症は、乳幼児期より皮下出血、筋肉内出血、関節内出血、頭蓋内出血、尿路出血などを認め、外傷や抜歯、手術後には止血困難を示します。
新生児期に臍出血を呈する症例もあります。
一方、プロトロンビン異常症のProthrombin Himiは無症状で出血の既往はありませんが、その他の症例では低下症と同様の出血症状を示します。
最近、アンチトロンビン(AT)との結合部位に異常を有するトロンビン異常が本邦から報告され、「AT抵抗性」による血栓性素因として注目されています。
検査所見
ホモ接合体や複合ヘテロ接合体例では、PT、APTTが著しく延長し、プロトロンビン活性はきわめて低い場合が多いです。
またプロトロンビン活性化の特殊な方法として、Staphylococcus aureusの菌体外蛋白質であるスタフィロコアグラーゼやEchis carinatus、Taipan等の蛇毒酵素をプロトロンビンアクチベーターとして用いる方法があります。
抗原量が低下しているものを低プロトロンビン血症、抗原量は正常であるが活性が低下しているものをプロトロンビン異常症と診断します。
中には、低プロトロンビン血症とプロトロンビン異常症の複合ヘテロ接合体などの場合があります。
治療
ホモ接合体で出血に対して迅速な治療が必要な場合や、手術前に予防投与する場合に、補充療法を行います。
本症の補充療法には、プロトロンビンを含む血漿由来第IX因子(FIX)複合体製劑を用います。
プロトロンビンは血漿中半減期が3日間と比較的長く、血漿プロトロンビン活性は20〜30%程度で止血レベルに入るため、30%を維持するように第IX因子複合体製劑20〜30 U/kgを投与します。
しかし、血栓症を合併する危険性があるので、150%以上を超えないように注意します。
後天性プロトロンビン低下症
後天性には、肝機能障害、ビタミンK(VK)欠乏、ワルファリン服用などにより低下しますので、鑑別の際に注意が必要です。
たとえば、新生児や乳幼児期にPT・APTTの延長を伴う出血傾向を認めたためVK欠乏症を疑い、VKの補充を行ったけれども効果が得られない場合は、先天性プロトロンビン欠損症などの存在も早期に考慮し、適切な検査および補充療法を開始すべきです。
また、後天性プロトロンビン低下症としてはまれですが、ループスアンチコアグラント・低プロトロンビン血症症候群(LA-HPS)についても、鑑別疾患の中に入れておく必要があります。
LAは臨床的には後天性の血栓症として重要ですが、まれに低プロトロンビン血症、あるいは血小板減少症や機能異常を合併した場合は出血します。
(続く) 先天性凝固異常症(4)第V因子欠乏/異常症へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:13
| 出血性疾患
先天性凝固異常症(2)先天性フィブリノゲン欠乏症
先天性凝固異常症(1)RBDより続く。
先天性凝固異常症(2)先天性フィブリノゲン欠乏症
先天性 Fbg欠乏症(無Fbg血症)/異常症
先天性無フィブリノゲン(Fbg)血症は、Fbgの合成障害により量的欠損をきたす出血性疾患で、発症頻度は100万人に1人と推定されます。
一方、先天性Fbg異常症はFbg構造異常により機能障害をきたし、これまでに世界で300症例以上の家系が報告されています。
症状
無Fbg血症の出血症状は、新生児期の臍出血から始まり、成長すると鼻出血、口腔内出血、過多月経、関節内出血などがしばしば認められます。
重篤な出血として頭蓋内出血をきたし、致死的となる場合もあります。
また、自然流産の原因となります。
Fbg異常症の約半数は無症候であり、約25%に出血傾向、約15%に血栓傾向を認め、一部には両者の合併例もあります。
まれに、出血・血栓・創傷治癒不全を示す症例もあります。
出血症状は軽度であり、鼻出血、過多月経、術後出血がみられます。
検査所見
無Fbg血症では、プロトロンビン時間(PT)、活性化部分トロンボプラスチン時間(APTT)、トロンビン時間(TT)はすべて著明に延長し、血小板粘着能やADP惹起血小板凝集も障害されます。
血漿中Fbg量は、凝固学的測定法(活性)と免疫学的測定法(抗原量)を比較し、同等に低下している場合は欠乏症と診断し、乖離している場合は異常症と診断します。
無Fbg血症では血漿Fbg量は10 mg/dl未満となります。
治療
止血治療には、Fbg製剤を用います。
通常Fbgの止血レベルは50 mg/dl以上ですが、安全に手術を行うために、100 mg/dl以上を止血・創傷治癒が完了するまで維持します。
Fbg製剤の半減期は2-4日ですが、手術時や出血時には消費により半減期が短縮することを考慮する必要があります。
また、妊婦や頭蓋内出血の既往がある患者には、Fbg製剤の定期的補充投与が推奨されます。
しかし、Fbg製剤の投与は血液由来感染症、血栓傾向、反復投与による抗体産生、アナフィラキシーショックなどの危険性があり、十分注意が必要です。
Fbg異常症で血栓症を発症した症例では、半永続的な経口抗凝固療法を行います。
(続く)先天性凝固異常症(3)先天性プロトロンビン低下/異常症へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:56
| 出血性疾患
先天性凝固異常症(1)RBD
先天性凝固異常症(1)RBD
はじめに
先天性出血性疾患の代表は血友病とvon Willebrand病(vWD)であり、平成23年度血液凝固異常症全国調査によると両者合わせて92%(血友病A 64%;4475例、血友病B14%;971例、vWD14%;984例)を占めています。
滝正志,他.血液凝固異常症全国調査,平成23年度報告書(財団法人エイズ予防財団).2012.
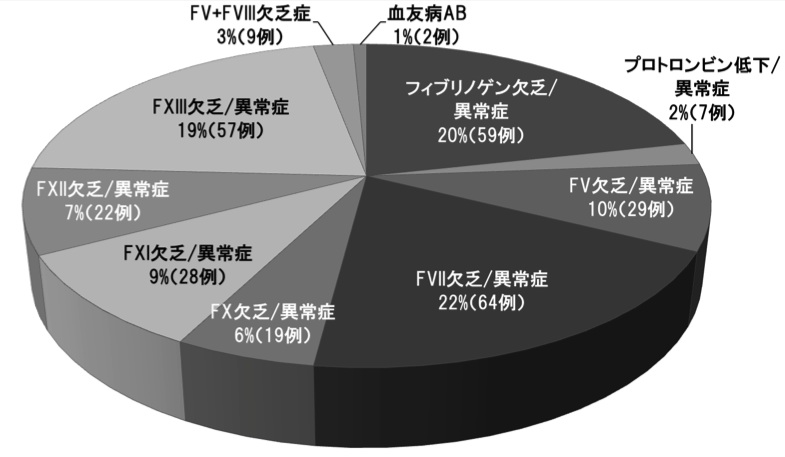
残りの8%(556例)程度が稀な凝固因子欠乏/異常症(rare bleeding disorders; RBD)です。
フィブリノゲン(Fbg)欠乏症/異常症、プロトロンビン低下/異常症、第V因子(FV)・第VII因子(FVII)・第X因子(FX)・第XI因子(FXI)・第XII因子(FXII)・第XIII因子(FXIII)欠乏/異常症、第V・VIII因子複合欠乏症があります。
本邦では、Fbg欠乏/異常症の頻度がRBDの22%と最も多く、次いでFVII欠乏/異常症(20%)、FXIII欠乏/異常症(19%)と続きます。
RBDは常染色体劣性遺伝形式をとり(Fgb異常症は常染色体優性遺伝)、ホモ接合体の発症頻度は50万から200万人に1人と極めて稀です。
Peyvandi F, Duga S, Akhavan S, Mannucci PM. Rare coagulation deficiencies. Haemophilia. 2002; 8: 308-321.
Mannucci PM, Duga S, Peyvandi F. Recessively inherited coagulation disorders. Blood. 2004; 104: 1243-1252.
Peyvandi F, Bolton-Mags PHB, Baltorova A, et al. Rare bleeding disorders. Haemophilia, 2012; 18: 148-153.
活性・抗原量ともに低下する欠乏症と、抗原量は正常であるが活性が低下する異常症に分類されます。
この後、Fbg、プロトロンビン、FV、FVII、FX、FXI、FXII、FXIII欠乏/異常症について概説します。
(続く)先天性凝固異常症(2)先天性フィブリノゲン欠乏症へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:34
| 出血性疾患
ホモシステイン
ホモシステイン
ホモシステインとは
ホモシステイン(Hcy)は、必須アミノ酸であるメチオニン代謝の中間代謝産物として生成されるチオール基を持つアミノ酸です。
代謝には、葉酸・ビタミンB6・ビタミンB12が関与しています。
先天性ホモシスチン尿症はまれな先天性代謝異常症の一つであり、Hcyを分解するシスタチオニンβ合成酵素の欠損により高Hcy血症をきたします。
患者は若年性の心筋梗塞、脳梗塞、深部静脈血栓症/肺塞栓(静脈血栓塞栓症:VTE)などの動・静脈血栓症を起こすことが知られています。この所見より、高Hcy血症と動脈硬化および血栓症との関連が注目されるようになり、最近の疫学研究では軽度の高Hcy血症でも心血管疾患の危険因子となることが明らかになりました。
動脈硬化、血栓症の発症機序としては、過剰なHcyにより血管内皮傷害をきたしTM、PC、PS系の抗凝固活性が低下したり、血小板が活性化されることが考えられています。
血中Hcy濃度も、血栓症精査の際にはスクリーニング検査として重要な項目です。
基準値
血中Hcy濃度は、生理的変動として加齢で増加します。
男性で高値であり、女性の場合閉経で上昇します。
血中総Hcy濃度 3.7〜13.5 nmol/mL (高速液体クロマトグラフィ:HPLC法)
通常血漿中では遊離型のHcyは1%程度とわずかで、70-80%が蛋白と結合した蛋白結合型Hcy、残りが二量体を形成したり他の低分子チオール化合物と結合した非結合型Hcyです。
血中Hcy濃度は、蛋白結合型と非結合型の総量として測定されます。
測定法には、HPLC法や酵素法があります。
異常となる病態・疾患
<血中Hcy濃度が高値を示す場合>
・生活習慣:喫煙 、コーヒー摂取
・Hcy代謝に必要なビタミンB12・B6、または葉酸欠乏
・先天性シスタチオニンβ合成酵素の欠損(ホモシスチン尿症)
・メチレンテトラヒドロ葉酸還元酵素(MTHFR)遺伝子の一塩基多型C677T
・腎障害
・先天性ホモシスチン尿症のホモ接合体では、血中Hcy濃度は基準値の10倍以上に増加しますが、ヘテロ接合体あるいはMTHFR遺伝子のC677T多型(TT型)では、軽度増加を示します。
(備考)
・葉酸、ビタミンB6、ビタミンB12の補充療法は、血中Hcy濃度を低下させますが、心血管疾患の発症リスクは低減させません。
Martí-Carvajal AJ, et al. Homocysteine-lowering interventions for preventing cardiovascular events. Cochrane Database Syst Rev. 2013
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:02
| 血栓性疾患
リポ蛋白(a) /Lp(a)
Lp(a)
リポ蛋白(a) [lipoprotein (a)]
LP(a)とは
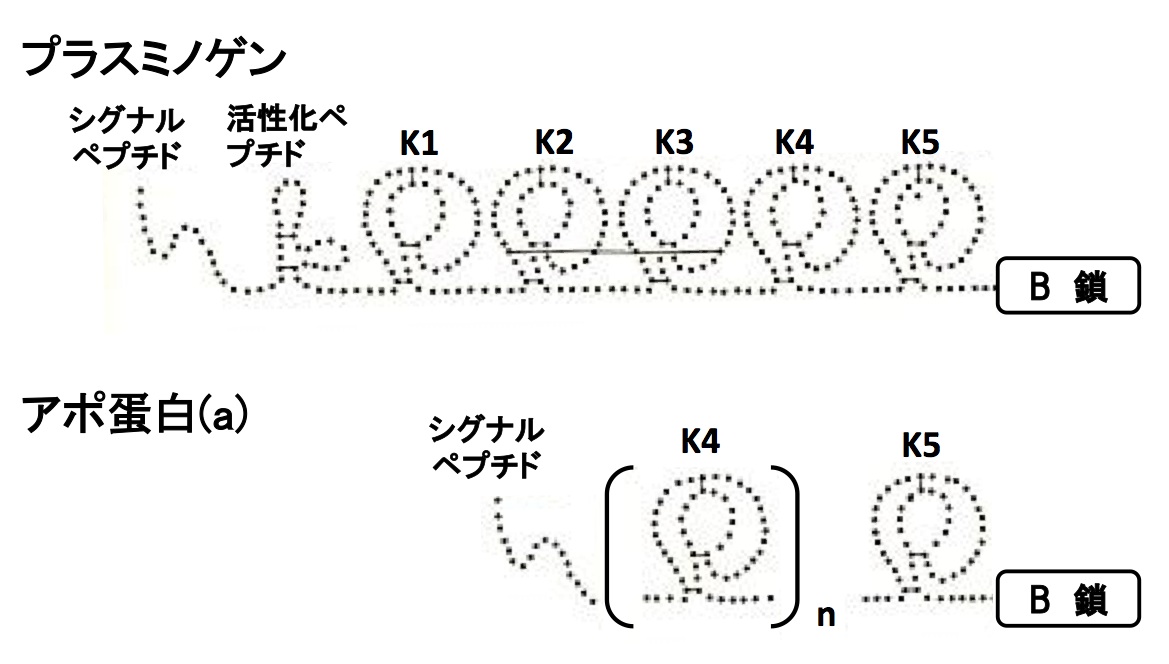
Lp(a)はLDLのアポ蛋白B-100にアポ (a)がS-S結合した脂質で、現在動脈硬化の独立した危険因子と考えられています。
アポ (a)は構造上プラスミノゲン(Plg)と極めて高い相同性を有し、Plgのクリングル4(K4)の繰り返し構造、K5およびセリンプロテアーゼ構造部分からなっています。
個人によってこのK4の繰り返し数(nは11から50)が異なるために分子量に多様性が生じ、Lp(a)の種々の表現型(フェノタイプ)が存在します。
アポ(a)の分子量の大きさと血清Lp(a)濃度は、ほぼ逆相関を示します。
動脈硬化の発症機序としては、Plgのフィブリンへの結合をLp(a)が競合的に阻害しプラスミン生成を抑制することにより線溶能が低下し、結果として動脈硬化に寄与すると考えられています。
Lp(a)濃度は優性遺伝し、一般人の1/4〜1/3が高Lp(a)血症を呈することより、先天性血栓性素因の一つと考えられています。
基準値
血清Lp(a)濃度は遺伝的素因で90%決まっており、環境要因の影響は少ないです。
新生児の血清濃度は成人の20-30%程度と低いですが、2歳までには成人値に達します。
成人以降の加齢の影響や性差については、報告によって異なります。
また、妊娠中期に上昇し、分娩時に正常値に戻ります。
血清濃度は個人差が大きく、0.1mg/dlから100mg/dlを超えるものまで1000倍以上濃度差があります。
その分布は低濃度領域に多い対数正規分布を示し白人と類似していますが、アジア系民族とは異なります。
基準値は30mg/dl(72nmo1/l)未満です。
Lp(a)の測定法は、一般的にはELISA法、免疫比濁法(TIA)、ラテックス免疫比濁法(LIA)が用いられています。
Lp(a)は凍結融解を繰り返すと変性しやすいため、測定値は低下します。
異常となる病態・疾患
・統計的に血清Lp(a)濃度が30mg/dl以上になりますと、動脈硬化の合併率が急激に増加し、冠動脈疾患、脳梗塞、閉塞性動脈硬化を発症しやすくなります。
・Lp(a)が低値となる場合の、臨床的意義は少ないです。
・高脂肪食後に若干低下します。
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:48
| 血栓性疾患
アミロイドーシスと出血(6)全身性アミロイドーシスの分類
アミロイドーシスと出血(5)病理より続く。
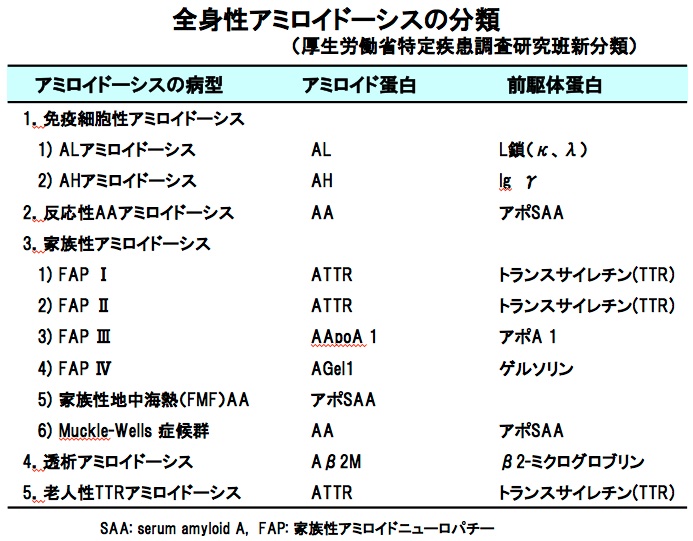
<アミロイドーシスと出血>(6)
全身性アミロイドーシスの分類(厚生労働省特定疾患調査研究班新分類)です。
(続く)アミロイドーシスと出血(インデックス)へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:12
| 出血性疾患
アミロイドーシスと出血(5)病理
アミロイドーシスと出血(4)第X因子低下&線溶活性化の症例より続く。
<アミロイドーシスと出血>(5)
注意点
・ALアミロイドーシスの出血傾向は、多岐にわたる要因により生じていますので、必ずしもFX活性値は出血の程度を反映しません。
また、FX活性値より、周術期の出血量を予測することは困難です。
Thompson CA,et al. Systemic AL amyloidosis with acquired factor X deficiency: A study of perioperative bleeding risk and treatment outcomes in 60 patients. Am J Hematol. 2010; 85: 171-3.
・ALアミロイドーシスの出血傾向では、APTT延長、FX活性低下に注目しやすいですが、線溶活性化にも着目し、血中α2-PIが低下しPICが著増しているような症例の止血治療には、抗線溶療法を試みると著効する場合があります。
アミロイドの病理所見
参照:腎生検の病理標本
Suzuki K. Diagnosis and treatment of multiple myeloma and AL amyloidosis with focus on improvement of renal lesion. Clin Exp Nephrol. 2012; 16: 659-71.
アミロイドは、病理学的にCongo red染色でオレンジ色に染まり、偏光顕微鏡で観察すると黄色または黄緑色の偏光を生じます。
電子顕微鏡で観察すると、幅 7〜15 mmの細長い線維が錯綜して存在しています。
(続く)アミロイドーシスと出血(6)全身性アミロイドーシスの分類へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:58
| 出血性疾患
アミロイドーシスと出血(4)第X因子低下&線溶活性化の症例
アミロイドーシスと出血(3)出血傾向の治療より続く。
<アミロイドーシスと出血>(4)
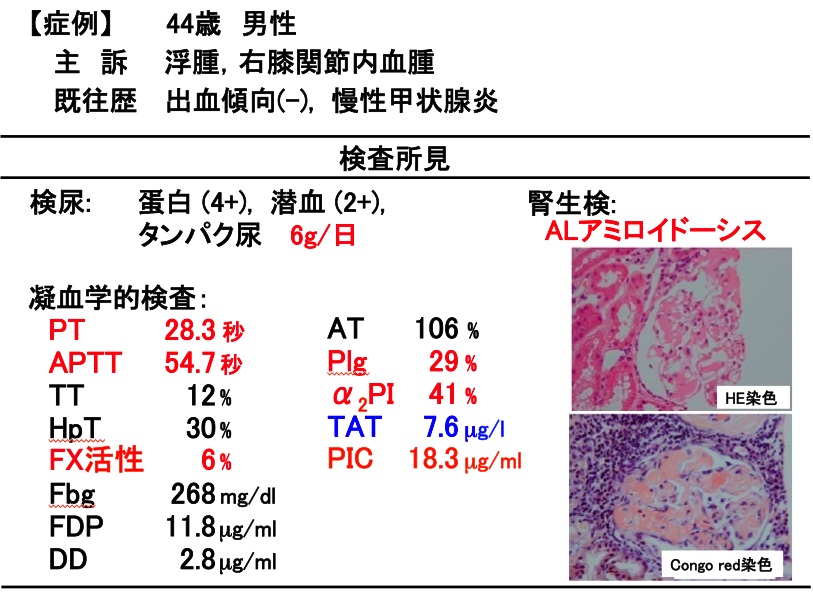
症例 44歳男性。
【主訴】下肢の著明な浮腫と右膝関節内血腫。
【現病歴】
生来健康で、出血傾向を認めない。
下肢のむくみと右膝関節痛・腫脹を認めたため近医を受診し、ネフローゼ症候群および膝関節内血腫と診断された。
腎生検の結果、ALアミロイドーシスと診断された。
【検査所見】
尿検査:蛋白4+、潜血2+
血液検査:PT 28.3秒、APTT 54.7秒、へパプラスチンテスト 30%、フィブリノゲン 268 mg/dl、FDP 11.8μg/ml、D−ダイマー 2.8μg/ml、アンチトロンビン活性 106%、プラスミノゲン活性 29%、α2プラスミンインヒビター 41%
TAT 7.6μg/l、PIC 18.3μg/ml、FX活性 6%。
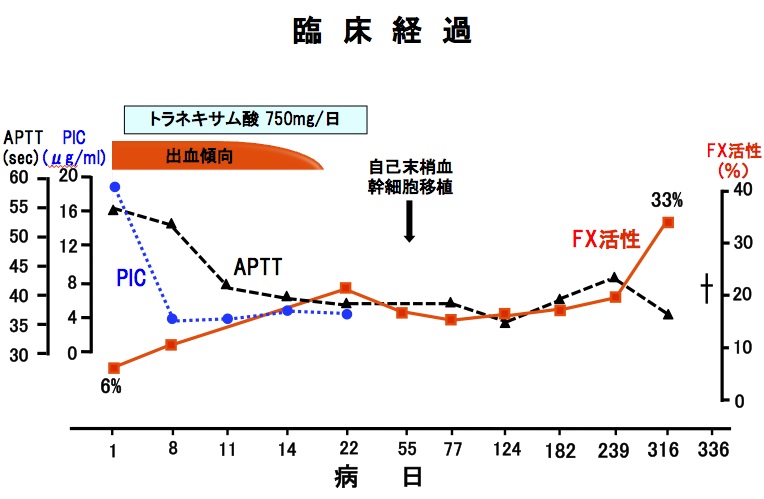
【入院後経過】
出血傾向に対して、抗プラスミン作用を有するトラネキサム酸投与を開始したところ、著明に亢進していた線溶活性は速やかに改善し(PIC 18.3→4.0μg/ml)、FX活性は徐々に改善して20%程度となり3週間後には出血傾向は消失しました。
ALアミロイドーシスの化学療法として、Auto-PBSCTを併用したメルファラン大量療法を施行したが根治には至らず、FX活性値は33%まで改善したが、最終的には発症11か月後に臓器不全にて永眠されました。
本症例の出血傾向は、FX活性低下に加えて線溶活性化の関与も大きいと考えられ、トラネキサム酸の投与だけで出血傾向が消失した点は注目すべきところでです。
(続く)アミロイドーシスと出血(5)病理へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:47
| 出血性疾患
アミロイドーシスと出血(3)出血傾向の治療
アミロイドーシスと出血(2)出血傾向の機序より続く。
<アミロイドーシスと出血>(3)
ALアミロイドーシス出血傾向の治療
出血傾向に対する治療としては、1)対症療法あるいは、2)ALアミロイドーシスそのものに対する治療を行います。
1)対症療法
線溶活性化が顕著な症例には、抗線溶療法が有効です。
代表的な抗線溶剤としてトラネキサム酸(商品名:トランサミン)がありますが、合成プロテアーゼインヒビターのメシル酸ナファモスタット(商品名:フサン)も抗凝固活性に加えて抗線溶活性を有しており、凝固・線溶両者が活性化されている症例では効果が期待できます。
後天性FX欠損症などの凝固因子低下例に対しては、脾摘や補充療法を行う場合があります。
補充療法はFFP輸注、VK製剤投与、デスモプレシン(DDAVP)、血漿交換などが行われますが効果は限られており、最近は活性型プロトロンビン複合体製剤(商品名:ファイバ)、遺伝子組換え活性型第VII因子製剤(商品名:ノボセブン)が使用されます。
特に、ノボセブンは突然発症した大出血時の止血管理に今後期待できるかもしれません。
2)ALアミロイドーシスそのものの治療
アミロイドーシスの出血傾向は、単一の凝固因子の欠損症である血友病などとは異なり、様々な要因が複雑に絡みあって発症しているため、最終的にはALアミロイドーシスを根本的に治療することが重要です。
近年は、完全寛解を目指しALアミロイドーシスの治療として、自己末梢血幹細胞移植(Auto-PBSCT)を併用したメルファラン大量療法などが行われており、完全寛解による異常細胞の消失に伴って出血傾向が消失し凝血学的異常所見が正常化する場合もあります。
(続く)アミロイドーシスと出血(4)第X因子低下&線溶活性化の症例へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:30
| 出血性疾患
アミロイドーシスと出血(2)出血傾向の機序
アミロイドーシスと出血(1)ALアミロイドーシスより続く。
<アミロイドーシスと出血>(2)
アミロイドーシスの出血傾向機序
ALアミロイドーシスでは、自然出血あるいは周術期の止血異常が約1/3(15〜41%)の患者で認められます。
主に、紫斑や点状出血、生検時の出血、さらには脳出血、消化管出血をきたします。
出血傾向をきたす機序としては、以下が考えられています。
1)凝固第X因子(FX)の低下(後天性FX欠損症)、まれにプロトロンビン、第V因子、第VII因子、第IX因子の低下、
2)線溶活性化
3)後天性von Willebrand症候群(AVWS)
4)フィブリン重合に対するインヒビターの出現
5)血小板機能異常による血小板凝集能の低下
6)消化管吸収不良性ビタミンK(VK)不足に伴うVK依存性凝固因子の低下
7)肝不全に伴う肝合成凝固因子の低下
8)アミロイド蛋白の沈着による血管の脆弱性
多数の要因が関与していると考えられていますが、それぞれについての詳細は不明な点が多いです。
Sucker C, et al. Amyloidosis and bleeding: pathophysiology, diagnosis, and therapy. Am J Kidney Dis. 2006; 47: 947-55.
Choufani EB, et al. Acquired factor X deficiency in patients with amyloid light-chain amyloidosis: incidence, bleeding manifestations, and response to high-dose chemotherapy. Blood. 2001; 97: 1885-7.
Thompson CA, et al. Systemic AL amyloidosis with acquired factor X deficiency: A study of perioperative bleeding risk and treatment outcomes in 60 patients. Am J Hematol. 2010; 85: 171-3.
Zangari M, et al, Hemostatic dysfunction in paraproteinemias and amyloidosis. Sem Thromb Hemost. 2007; 33: 339-49.
1)後天性FX欠損症は、ALアミロイドーシスの8.7%〜14%で認められます。その発症機序は、FXがアミロイド蛋白への親和性が高いためアミロイド沈着部位に吸着されてしまい、その結果循環血漿中から速やかにクリアランスされる、と考えられています。
アフィニティークラマトグラフィーを用いた解析によると、FXはしばしば脾臓のアミロイド繊維に結合しており、脾摘が出血傾向の改善に有効であったとの報告があります。
2)線溶活性化は、形質細胞におけるウロキナーゼ(u-PA)産生過剰、α2プラスミンインヒビター活性の低下、などが関与すると報告されており、プラスミノゲン活性低下、プラスミン・α2プラスミンインヒビター(PIC)高値、FDPの増加が検査所見として認められます。
3)AVWS発症機序としては、アミロイド繊維または形質細胞表面に選択的に高分子von Willebrand因子(VWF)マルチマーが吸着されるか、あるいは分解される可能性が考えられています。
VWFマルチマー解析では高分子VWFが欠落しており、リストセチンコファクター活性(VWF:RCo)が低下します。
5)〜8)一方、アミロイド蛋白は、腎臓、消化管、肝臓、血管など、様々な臓器に沈着し障害をきたします。
さらに、凝血学的異常所見としては、凝固活性化による血中トロンビン産生の増加を示すトロンビン・アンチトロンビン複合体(TAT)が高値を示す場合が、しばしばあります。
また、血中フィブリノゲン値は、骨髄腫に伴うサイトカイン誘導により急性反応性蛋白として増加する症例が約半数あり、一方で肝不全による産生障害、凝固活性化による消費、線溶活性化による分解により、低下をきたす場合もあります。
(続く)アミロイドーシスと出血(3)出血傾向の治療へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:13
| 出血性疾患
アミロイドーシスと出血(1)ALアミロイドーシス
<アミロイドーシスと出血>(1)
アミロイドーシスとは
アミロイドーシス(amyloidosis)とは、「アミロイド」という難溶性で繊維状の異常蛋白が、全身臓器に沈着することによって機能障害を引き起こす予後不良の疾患群です。
発症機序としては、まず”アミロイド前駆体蛋白”が作られ(その生成過程は依然として詳細不明です)、それがプロセシングを受け、重合、凝集して“アミロイド蛋白”を形成します。
全身の複数の臓器にアミロイド蛋白が沈着する「全身性アミロイドーシス」と、特定の臓器に限局して沈着する「限局性アミロイドーシス」とに分類され、さらに前駆体蛋白とアミロイド蛋白によって臨床病型が分かれます。
全身性アミロイドーシスでは出血傾向をきたすことが知られており、特に「免疫細胞性アミロイドーシス(ALアミロイドーシス)」における凝血学的異常所見は臨床的にも重要です。
免疫細胞性アミロイドーシス(ALアミロイドーシス)
免疫細胞性アミロイドーシスは、免疫グロブリン軽鎖(κ、λ)を前駆体としたAL(amyloidogenic L chain)アミロイドが全身臓器に沈着して発症する疾患で、異常形質細胞のクローン性増殖による形質細胞増殖性疾患の一種です。
骨髄腫に合併(骨髄腫ないしマクログロブリン血症に伴うAL型アミロイドーシス)して起こることもありますが、骨髄腫の診断基準を満たさない場合のほうが多いです。
症状は、アミロイドの沈着による臓器・組織の障害により発生するため多彩ですが、不整脈や心不全(心臓に沈着)、ネフローゼ症候群や腎不全(腎に沈着)、胃腸障害、肝障害(消化器系臓器に沈着)、手足のしびれや立ちくらみ・麻痺・排尿障害(末梢神経および自律神経障害)などがしばしば認められます。
(続く)アミロイドーシスと出血(2)出血傾向の機序へ
<リンク>:臨床に直結する血栓止血学
投稿者:血液内科・呼吸器内科at 01:01
| 出血性疾患
「臨床に直結する血栓止血学」発刊のご案内
「臨床に直結する血栓止血学」(中外医学社)が、本年の10月に発刊されます。
リンク1:臨床に直結する血栓止血学
リンク2:臨床に直結する血栓止血学
血栓止血の専門医40人以上による、臨床に直結するを意識した書籍です。
日本血液学会では、学会会場で展示販売される予定です。
発刊に先立って、「臨床に直結する血栓止血学」の序を紹介させていただきます。
序
血栓止血学というと、どちらかといえば取っ付きにくい領域と思われてきました。しかし、実は決して難しい領域ではなく、いかに楽しく、一旦理解してしまえば記憶することも少ないとても興味深い領域であることが本書を読めば分かっていただけると思います。
近年、出血性疾患、血栓性疾患ともに病態、検査・診断、治療の各面で新たな展開がみられています。薬剤も、新規経口抗凝固薬(ダビガトラン、リバーロキサバン、エドキサバン、アピキサバン)、遺伝子組換えトロンボモジュリン製剤、エクリズマブなどが次々と登場しました。血栓止血領域の臨床がかつてないくらい脚光を浴びている今、本書の果たす役割は大きいのではないかと思います。
血栓止血学の基礎から詳細に論じた専門書や雑誌は多数ありますが、本書はあくまでも「臨床に直結する」を意識しています。換言いたしますと臨床に直結するとまでは言えない基礎的事項は思い切って割愛して、そのぶん臨床的な内容を充実させています。血栓止血の臨床をしみじみと分かっていただくための入門書です。
教科書的な基本知識にとどまらず、以下の内容を充実させています。
・ ここがコンサルトされやすい!
・ ピットフォール
・ お役立ち情報
・ 症例紹介:各疾患のイメージがクリアになると思います。
血栓止血の臨床において血液凝固検査の適切な評価は最重要です。凝血学的検査を極めれば、血栓止血の臨床の8割以上は極めたと言えるかもしれません。各疾患や薬剤の章でも凝血学的検査の話は登場しますが、まず検査の章を最初に組んであるのは、凝血学的検査の重要性を認識しているためです。
想定している読者は血栓止血のエクスパートではなく、以下の皆さんです。
・ 研修医、一般臨床医
・ 血液専門医(ただし血栓止血専門以外)、血液以外の専門医(特に、循環器内科、脳外科、心臓血管外科、救急部・集中治療部、臨床検査医学、神経内科など)
・ 臨床検査技師、薬剤師
・ 医学生、保健学科学生
本書を手にした皆さんが、血栓止血の臨床に興味を持っていただき、日本におけるこの領域のレベル向上がもたらされることを願っています。
<リンク>
投稿者:血液内科・呼吸器内科at 01:50
| 研修医の広場
北陸 Expert Meeting:抗血栓療法、NOAC、心房細動
北陸 Expert Meeting
日時;2013年9月26日(木) 19:00〜21:15
会場:ANAクラウンプラザホテル金沢 3階 鳳の間
総合座長
金沢大学医薬保健研究域医学系 恒常性制御学 教授
金子 周一 先生
基調講演
座長
金沢大学医薬保健域医学系 細胞移植学 教授
中尾 眞二
演者
1)金沢大学附属病院 高密度無菌治療部 准教授
朝倉 英策
「抗血栓療法の歩み」
演者
2)金沢大学医薬保健研究域保健学系 病態検査学 教授
森下 英理子
「抗凝固薬と血液凝固系検査」
特別講演
座長
金沢大学附属病院 循環器内科 講師
高村 雅之 先生
演者
心臓血管研究所 所長・付属病院長
山下 武志 先生
「いっせいにNOACが野に放たれた今、私が考えること」
主催:日本ベーリンガーインゲルハイム株式会社
<リンク>
投稿者:血液内科・呼吸器内科at 01:34
| 研究会・セミナー案内
感染症治療Up to Date 2013 in 石川 の御案内
感染症治療Up to Date 2013 in Ishikawa
日時 :2013年9月20日(金) 18:40 〜 20:40
場所 :金沢都ホテル 7階 鳳凰の間
PROGRAM
情報提供 18:40〜19:00
『呼吸器感染症におけるグレースビット錠の有用性について』 第一三共株式会社 福田 聰
開会挨拶 19:00〜19:05
金沢大学医薬保健研究域医学系細胞移植学 准教授 笠原 寿郎
一般講演 19:05〜19:35
座長:金沢医科大学 臨床感染症学 教授 飯沼 由嗣 先生
講演1『当院におけるクラビット点滴静注の使用経験』
金沢社会保険病院 呼吸器内科 部長 渡辺 和良 先生
講演2『高齢者施設(特養)における気道感染症に対するグレースビットの使用経験』
三宅医院 院長 三宅 靖 先生
特別講演 19:35〜20:35
座長:国立病院機構 七尾病院 院長 藤村 政樹 先生
『呼吸器感染症に対する抗菌薬の適正使用』
信楽園病院 研究部長 青木 信樹 先生
閉会挨拶 20:35〜20:40
金沢医科大学 呼吸器内科学 教授 栂 博久 先生
※ 当講演会は、石川県病院薬剤師会の後援を頂き、石川県病院薬剤師会生涯研修制度 ≪1単位≫
に該当いたします
主催:第一三共株式会社
後 援:石川県病院薬剤師会
<リンク>
投稿者:血液内科・呼吸器内科at 01:27
| 研究会・セミナー案内
血液内科試験:貧血、血小板数低下など
平成25年度 内科学卒業試験(BSL評価試験)血液内科学
平成25年9月10日(火)
5. 60歳の女性。
半年前から全身倦怠感と労作時の息切れが出現。検診で貧血と白血球減少を指摘されたため来院した。50歳時に乳がんのため化学療法を受けている。その後乳がんの再発は認めていない。
血液所見:赤血球数200万,Hb 7.0 g/dl,Ht 22%,白血球数2,000(好中球数1,400、芽球なし)、血小板数4万。骨髄塗抹標本をスライド5に示す(省略)。
この疾患について正しいのはどれか。
(1) 7番染色体異常を伴うものは予後不良である。
(2) 5q-陽性例は日本では稀である。
(3) 骨髄中の鉄芽球が多ければ診断できる。
(4) 60歳以上では同種骨髄移植の適応はない。
(5) 5q-陽性例ではレナリドマイドが奏効する。
a (1), (2), (3) b (1), (2), (5) c (1), (4), (5) d (2), (3), (4) e (3), (4), (5)
6. 18歳の男性。
息切れ、口腔内出血を主訴に来院し入院となった。入院時身体所見で眼瞼結膜は貧血様で四肢に紫斑を認めた。
検査所見:RBC 201万、Hb 6.7 g/dL、Ht 19.9%、WBC 800、Plt 1.1万、直接ビリルビン 0.6 mg/dL、AST 34 IU/L、ALT 35 IU/L、LDH 722 IU/L、 APTT 35秒(対照 28.8秒)、フィブリノーゲン 85 mg/dL、FDP 62 μg/mLであった。
骨髄塗抹標本ではスライド6(省略)に示すような細胞を85%認めた。この患者でみられやすい染色体異常はどれか。1つ選べ。
a. t(1;19)(q23;p13)
b. t(8;21)(q22;q22)
c. t(15;17)(q22;q11)
d. t(9;22)(q34;q11)
e. t(8;14)(q24;q32)
7. 58歳の男性。
健康診断で著明な白血球増加を指摘された。
血液検査所見:WBC 76,000/μL (骨髄芽球 1.2%、前骨髄球 5.8%、骨髄球 15.8%、後骨髄球 8.6%、桿状核好中球 13.8%、分葉核好中球 44.2%、好塩基球 3.2%、リンパ球 3.2%、単球 3.4%)、Hb 11.5 g/dL、Plt 72.1万/μL。
骨髄塗抹標本をスライド7に示す(省略)。診断確定に必須の検査はどれか。一つ選べ。
a. ミエロペルオキシダーゼ染色
b. エステラーゼ二重染色
c. 表面マーカー検査
d. 骨髄生検
e. 染色体検査
(正答)
5:b
6:c
7:e
<リンク>
投稿者:血液内科・呼吸器内科at 01:35
| 医師国家試験・専門医試験対策
血液内科試験:白血球増多
平成25年度 内科学卒業試験(BSL評価試験)血液内科学
平成25年9月10日(火)
50歳の男性。
平成25年1月近医で白血球増多を指摘されたが、無症状であったため放置していた。6月より腰痛が出現し、嘔気・全身倦怠感が著明となったため緊急入院となった。
身体所見:両側頸部・腋窩に1cm大のリンパ節を触知。貧血、肝脾腫などはない。
検査所見:赤血球数475万、Hb 15.1g/dl、Ht 44.0%、白血球数33,300(好中球41%、リンパ球9%、単球5%、好酸 1%、異型リンパ球 44%)、血小板数17.9万、網赤血球3.8万、Na 141mEq/l、K 4.1 mEq/l、Cl 96 mEq/l、Ca 14.6 mg/dl、LDH 671 IU/l (基準値120-214)、可能性インターロイキン2受容体23,100 U/ml。
末梢血塗抹標本像をスライド4に示す(省略)。
4-1.本症に多い合併症はどれか。
(1) 皮膚病変
(2) 消化管出血
(3) 歯肉腫帳
(4) 日和見感染症
(5) 高カルシウム血症
a (1), (2), (3) b (1), (2), (5) c (1), (4), (5) d (2), (3), (4) e (3), (4), (5)
4-2.本症に関する記載として正しいものはどれか。
(1) 若年者に発症のピークがある。
(2) 授乳による垂直感染が主な原因である。
(3) 抗CCR4抗体(モガムリズマブ)が有効である。
(4) 化学療法後の予後は不良である。
(5) ウイルス感染者のほとんどが本症を発症する。
a (1), (2), (3) b (1), (2), (5) c (1), (4), (5) d (2), (3), (4) e (3), (4), (5)
(正答)
4-1:c
4-2:d
<リンク>
投稿者:血液内科・呼吸器内科at 01:26
| 医師国家試験・専門医試験対策
血液内科試験:貧血と赤血球
平成25年度 内科学卒業試験(BSL評価試験)血液内科学
平成25年9月10日(火)
25歳の女性。
2年前の健康診断で軽度の貧血を指摘されたが放置していた。2週間前に風邪をひいたため近医を受診した際に総合感冒薬を処方された。発熱・筋肉痛は改善したが全身倦怠感が持続するため内科を受診した。
家族歴として、母が胆嚢と脾臓の摘出術を受けており、姉は検診で貧血を指摘されている。
身体所見:眼瞼結膜は貧血様、球結膜に黄疸を認める。表在リンパ節は触知しない。弾性軟の肝を1.5横指、脾を1横指触知する。
血液所見:赤血球数220万、Hb 6.7 g/dl、Ht 18%、白血球数8,600(好中球数6,400)、血小板数18.9万、網赤血球0.5万、LDH 320 IU/l (基準値120-214)、総ビリルビン 2.5 mg/dl、直接ビリルビン0.5 mg/dl。末梢血塗抹標本像をスライド3に示す(省略)。
3-1. 本症の診断に有用な検査はどれか。
(1) NAPスコア
(2) 赤血球浸透圧脆弱性試験
(3) 血清中パルボウイルスB19抗体価
(4) 骨髄穿刺
(5) 血清中ビタミンB12値
a (1), (2), (3) b (1), (2), (5) c (1), (4), (5) d (2), (3), (4) e (3), (4), (5)
3-2 本症の治療として適切でないものはどれか。
(1) 副腎皮質ステロイド
(2) 脾摘
(3) 輸血
(4) 抗C5モノクローナル抗体(エクリズマブ)
(5) 造血幹細胞移植
a (1), (2), (3) b (1), (2), (5) c (1), (4), (5) d (2), (3), (4) e (3), (4), (5)
(正答)
3-1:d
3-2:c
<リンク>
投稿者:血液内科・呼吸器内科at 01:18
| 医師国家試験・専門医試験対策
血液内科試験:リンパ節腫脹
平成25年度 内科学卒業試験(BSL評価試験)血液内科学
平成25年9月10日(火)
64歳の女性。
3か月前から38.5 ℃程度までの発熱と軽度の腹痛があり、軽快と増悪を繰り返していた。発熱の際にはひどい盗汗と全身倦怠感を認めた。
近医を受診したところ、血液検査でCRPの上昇と赤沈の亢進がみられたが原因は不明であった。
1か月前から左頚部に1 cm大の腫瘤があることに気付いた。最近になって徐々に増大してきたため内科を受診した。この7か月で体重は47 kgから40 kgに減少していた。
身体所見:左側頚部に2 cm大、3 cm大のリンパ節をそれぞれ1個触知する。弾性硬、可動性は良好で圧痛はない。右頚部、鎖骨窩、腋窩、鼡径部などにリンパ節は触知しない。
血算には異常を認めない。LDH 363 IU/l、CRP 12.6 mg/dl、可溶性インターロイキン2受容体 3,360 U/mlであった。
頸部リンパ節生検のH-E染色標本をスライド2に示す(省略)。
2-1. 本症例について正しいのはどれか。
(1) 生検標本上の大型の細胞はランゲルハンス巨細胞である。
(2) 大型細胞の起源はB細胞である。
(3) EBウイルスが発症に関与している。
(4) ツベルクリン反応は陰性化することが多い。
(5) 発熱は稽留熱であることが多い。
a (1), (2), (3) b (1), (2), (5) c (1), (4), (5) d (2), (3), (4) e (3), (4), (5)
2-2. 全身CT・FDG-PETでは左頸部、縦隔のリンパ節腫大に加えて脾腫が認められた。この患者に対して行われる可能性の高い治療はどれか。一つ選べ。
a. 副腎皮質ステロイド
b. 頚部・縦隔に対する放射線照射+摘脾
c. ABVD療法
d. R-CHOP療法
e. リツキシマブ単独療法
(正答)
2-1:d
2-2:c
<リンク>
投稿者:血液内科・呼吸器内科at 01:12
| 医師国家試験・専門医試験対策
血液内科試験:貧血
平成25年度 内科学卒業試験(BSL評価試験)血液内科学
平成25年9月10日(火)
28歳の女性。
生来健康であり、これまでの血液検査で異常を指摘されたことはなかった。約2か月前から全身倦怠感を自覚していた。倦怠感の増悪とともに労作時の息切れも自覚するようになったため内科を受診した。
初診時現症:顔面蒼白、眼瞼結膜 貧血様、眼球結膜 軽度黄染。心音・肺音 異常なし。腹部所見異常なし。
検尿:蛋白(−)、潜血反応(−)、糖(−)、ウロビリノーゲン(++)、ビリルビン(+)、沈渣 異常なし。
血液所見:赤血球数240万、Hb 8.2 g/dl、Ht 26.4%、白血球数4,300、血小板数4.6万、網赤血球25.4万、LDH 748 IU/l、総ビリルビン 2.4 mg/dl、直接ビリルビン0.7 mg/dl、ハプトグロビン<10 mg/dl。骨髄塗抹標本をスライド1(省略)に示す。
1-1. 本疾患を診断するためにさらに行うべき検査項目はどれか。
(1) 抗核抗体
(2) 可溶性インターロイキン2受容体
(3) 塗抹標本のペルオキシダーゼ染色
(4) 寒冷凝集素
(5) クームス試験
a (1), (2), (3) b (1), (2), (5) c (1), (4), (5) d (2), (3), (4) e (3), (4), (5)
1-2. この臨床経過・検査結果から否定できる疾患はどれか。
(1) 悪性貧血
(2) エバンス症候群
(3) 発作性夜間血色素尿症
(4) 急性骨髄単球性白血病
(5) 赤白血病
a (1), (2), (3) b (1), (2), (5) c (1), (4), (5) d (2), (3), (4) e (3), (4), (5)
(正答)
1-1:c
1-2:c
<リンク>
投稿者:血液内科・呼吸器内科at 01:06
| 医師国家試験・専門医試験対策
血液内科試験:インフォームド・コンセントなど
平成25年度 内科学卒業試験(BSL評価試験)血液内科学
平成25年9月10日(火)
骨髄移植に関するインフォームド・コンセントを患者から得るために、担当医が取るべき態度はどれか。3つ選べ。
a. 患者への説明内容は、事前に家族と相談しておく。
b. 骨髄移植の方法とそれによる利益(効果)・不利益(危険性)を説明する。
c. 骨髄移植を受けなかった場合の不利益を説明する。
d. 骨髄移植以外の代替治療について、その方法と利益・不利益を説明する。
e. 患者の不安をあおる合併症の説明は避ける。
(正答) b, c, d
副腎皮質ステロイド大量療法を受けた患者に通常はみられない副作用はどれか。1つ選べ。
a. 消化性潰瘍
b. 骨粗鬆症
c. 高血糖
d. 末梢神経障害
e. 精神障害
(正答) d
抗がん剤投与を受けている患者の発熱性好中球減少症に対する初期治療として適切な薬剤はどれか。2つ選べ。
a. ペニシリンG
b. バンコマイシン
c. セフェピム(第4世代セフェム系)
d. メロペネム(カルバペネム系)
e. クラリスロマイシン(マクロライド系)
(正答) c, d
<リンク>
投稿者:血液内科・呼吸器内科at 01:00
| 医師国家試験・専門医試験対策
血液内科試験:白血病など
平成25年度 内科学卒業試験(BSL評価試験)血液内科学
平成25年9月10日(火)
診断と治療の組み合わせが誤っているのはどれか。2つ選べ。
a. CBF(core binding factor)関連急性骨髄性白血病 − 大量シタラビン
b. フィラデルフィア染色体陽性急性リンパ性白血病 − イマチニブ
c. 慢性骨髄性白血病骨髄性急性転化 − VP療法(ビンクリスチン+プレドニゾロン)
d. 本態性血小板血症 − 瀉血
e. 多発性骨髄腫 − ボルテゾミブ
(正答) c, d
疾患名と検査結果の組み合わせで誤っているのはどれか。2つ選べ。
a. 最未分化型急性骨髄性白血病(FAB分類:M0) − ミエロペルオキシダーゼ染色陰性
b. 急性前骨髄球性白血病 ― FDP高値
c. 急性単球性白血病 ― 血清リゾチーム高値
d. 急性リンパ性白血病 ― Auer小体
e. 慢性骨髄性白血病 ― JAK2遺伝子変異
(正答) d, e
原発性骨髄線維症に特徴的ではない所見はどれか。1つ選べ。
a. 巨大脾腫
b. 末梢血中の好塩基球増多
c. 末梢血に赤芽球出現
d. 涙滴赤血球
e. 骨髄穿刺時におけるdry tap
(正答) b
血清蛋白電気泳動にてM蛋白を呈さない疾患はどれか。1つ選べ。
a. 多発性骨髄腫
b. 原発性アミロイドーシス
c. 原発性マクログロブリン血症
d. POEMS症候群
e. 全身性Castleman病
(正答) e
<リンク>
投稿者:血液内科・呼吸器内科at 01:51
| 医師国家試験・専門医試験対策
血液内科試験:輸血学
平成25年度 内科学卒業試験(BSL評価試験)血液内科学
平成25年9月10日(火)
同種骨髄移植を行う際、移植(輸注)する骨髄液から血球除去が不必要なドナー/レシピエントの血液型組合せはどれか。一つ選べ。なお、A+はA型RhD陽性を指す。
a. A+/B+
b. B+/A+
c. AB+/A+
d. A+/AB+
e. O+/O-
(正答)d
造血幹細胞移植後の移植片対宿主病(GVHD)に関する下記の記述について、誤っているのはどれか。一つ選べ。
a. 急性GVHDは移植後100日以内に起こりやすい。
b. 慢性GVHDは移植後100日以降に起こりやすい。
c. 急性GVHDの主な標的臓器は、皮膚・肝・腸管である。
d. GVHDの標準予防法は、シクロスポリン(またはタクロリムス)+短期メトトレキセート療法である。
e. HLA一致同胞間骨髄移植後急性GVHDとHLA一致非血縁者間骨髄移植後急性GVHDの頻度は同じである。
(正答)e
アルブミンの不適切使用例はどれか。一つ選べ。
a. 重症熱傷
b. 出血性ショック
c. 蛋白質源としての栄養補給
d. 人工心肺を使用する心臓手術
e. 肝硬変に伴う難治性腹水に対する治療
(正答)c
輸血に関して正しいのはどれか。一つ選べ。
a. 輸血した血小板の1/10は脾臓で捕捉される。
b. 新鮮凍結血漿製剤は融解後3時間以内に輸注する。
c. 造血幹細胞移植時の輸血療法は、血小板輸血より赤血球輸血が中心となる。
d. Corrected count increment (CCI)の計算は、赤血球輸血効果の評価に役立つ。
e. 体重40 kgの患者に赤血球製剤を2単位輸血すれば、Hbは約1 g/dL上昇する。
(正答)b
<リンク>
投稿者:血液内科・呼吸器内科at 01:46
| 医師国家試験・専門医試験対策
血液内科試験:凝固検査
平成25年度 内科学卒業試験(BSL評価試験)血液内科学
平成25年9月10日(火)
血栓止血関連マーカーの変動を示した下記の記載のうち正しいものはどれか。一つ選べ。
投稿者:血液内科・呼吸器内科at 01:15
| 医師国家試験・専門医試験対策