厚生労働省DIC診断基準の改訂へ
理想のDIC診断基準とは?
播種性血管内凝固症候群(DIC)診断基準を論ずる場合には、DICの概念をどう考えているかを明確にしておく必要があります。
海外では、DICの基礎疾患として敗血症などの重症感染症のみを想定した疾患概念が多いように思われます。
しかし、DICの基礎疾患としては、急性白血病、固形癌、大動脈瘤など多くが知られており、どのような基礎疾患であっても通用する疾患概念であることが望まれます。
DICの概念は以下のようにまとめられると思います。
1)基礎疾患の存在
2)全身性持続性の著明な凝固活性化
3)線溶活性化(その程度は基礎疾患により種々)
進行した場合には
4)消費性凝固障害
5)臨床症状(出血症状・臓器層状)に出現
(4)5)はDICであるための必要条件ではないとする考え方です)。
理想のDIC診断基準に求められる条件として、以下を挙げることができると思います。
1)全ての基礎疾患に適用できること
2)DICの本態を評価していること
3)治療に直結していて患者の予後を改善できること
4)誤診されないこと
厚生労働省DIC診断基準は、長年にわたり使用されてきた実績のある診断基準ですが、多くの問題点も指摘されてきました。
厚生労働省DIC診断基準の問題点は、具体的には以下です。
1)臨床の現場では6点(白血病群では3点)で治療開始されており実情に合わない
2)基礎疾患ありでのスコアリングはナンセンス
3)臨床症状でのスコアリングは早期診断に悪影響(DICによる症状であることの鑑別も不可能)
4)PTはDICに特異的なマーカーでない
5)DICの本態である凝固活性化マーカーが含まれていない
6)誤診される症例の多くはFDPが10μg/mL未満であること、など。
また、多様な病態を示す各種基礎疾患に合併したDICを単一の基準で診断することの限界も指摘されています。
基本となるDIC診断基準とは別に骨髄抑制群、感染症群、肝不全群などに対応する診断基準もあった方が良いという考え方もあると思います。
DIC診断基準に凝固活性化を反映する分子マーカー(TATなど)を組み込むことにとって、分子マーカーが更に普及して、日本におけるDIC診療レベルの向上につながることにも期待したいと思います。
なお、今回の記事は、管理人の私見ですので、異論もあると思っています。
<リンク>
投稿者:血液内科・呼吸器内科at 01:19
| DIC
新規経口抗凝固薬(プラザキサ、リクシアナ、リバロキサバンなど)
ダビガトラン(商品名:プラザキサ)、エドキサバン(商品名:リクシアナ)、リバロキサバンなどの新規経口抗凝固薬は、ワルファリン(PT-INR)に代わる画期的な抗凝固薬として、大変に期待されています。
スーパーワルファリンと言っても良いと思います。
このような素晴らしいお薬は、大事に育てる必要があるのではないでしょうか。その観点から、モニタリング(血液凝固検査)の意義はとても大きいのではないかと思っています。
これらの新規経口抗凝固薬は、循環器領域、脳卒中領域、血栓止血学、臨床検査医学などいろんな領域で話題になっています。
抗血栓療法には、抗血小板療法と抗凝固療法があります。
抗血小板薬は血小板活性化を主病態とした血栓症(動脈血栓症)に処方され、抗凝固薬は凝固活性化を主病態とした血栓症(静脈血栓症)に処方されます。
抗凝固薬は、具体的には静脈血栓塞栓症(深部静脈血栓症、肺塞栓)の再発予防や、心房細動に起因する心原性脳塞栓の発症予防目的として、不可欠の重要な薬物です。
経口可能な抗凝固薬としては、長年にわたりワルファリンのみが用いられてきました。
ワルファリンはビタミンK依存性凝固因子活性を抑制することにより、抗凝固活性を発揮します。
我が国においては、歴史的にはトロンボテストによるコントロールが行われてきたが、世界的な大規模臨床試験はPT-INR(PT-INR検査)によるモニタリングで評価されてきた報告がほとんどですから、我が国においてもPT-INRによるモニタリングが主流になってきました。
しかし、トロンボテストはフィブリノゲンや第V因子の影響を受けずにビタミンK依存性凝固因子であるVII、X、II因子のみに依存しているという利点もあります。
フィブリノゲン上昇を伴う炎症反応時などにも信頼できる点や、先天性第V因子欠損症にワルファリンコントロールを行っている症例にも使用可能である点は念頭におきたいと思います。
ワルファリン内服時にモニタリングされるPT-INRですが、PT-INRが著しく上昇した症例では大出血をきたしやすいことは数々の報告から明らかですが、PT-INRが高値であっても、なお血栓症を発症しやすいことにも留意する必要があります。
すなわち、PT-INRは出血の副作用チェックの意義は大きくても、必ずしも効果判定のマーカーにはなりえないことがありますので、今後の検討課題と考えられます。
近年、経口可能な抗凝固薬(新規経口抗凝固薬)として、トロンビン阻害薬(プラザキサ)、Xa阻害薬が登場しました。
大規模臨床試験の結果から、これらの薬物はワルファリンより効果の点で上回り、副作用も少ない点で期待が寄せられました。
加えて、ワルファリンのように頻回の採血によるモニタリングが必要ない点が当初キャッチフレーズとなりました。
しかし、実臨床の場で広く処方されるようになりますと、予想以上に出血の副作用がみられることが話題になり(特に腎障害例や高齢者など)、そのモニタリングをどうするか議論となっています。
新規経口抗凝固薬におけるモニタリングをどうするかについて議論する場合に、以下のようないくつかの注意点があります。
【新規経口抗凝固薬モニタリングの注意点】
1)薬物の血中濃度によってPTやAPTTの延長度が異なるために、内服から採血時間までの配慮が必要なこと(血中濃度がピークの時点で採血すべきと考えられます)。
2)同じサンプルであっても試薬の種類によって大きくデータが変わる場合があること。
3)新規経口抗凝固薬の種類によってPTまたはAPTTのどちらが延長しやすいかが異なること。
さらに、PTやAPTTは新規経口抗凝固薬の出血のモニタリングとしての価値はある可能性がありますが、効果判定のマーカーにはならないかも知れません。
副作用、効果判定はそれぞれ違ったマーカーによるモニタリングが必要となるのではないかと考えられます。
新規経口抗凝固薬は、人類が待ち望んだ優れた薬物です。
これらの薬物が大きく育つためにも、モニタリングの意義はとても大きいのではないかと考えられます。
追伸:今回の記事は、管理人の私見です。反対意見も当然あると思いますし、今後の検討課題がたくさんあるのではないかと思っています。
<リンク>
投稿者:血液内科・呼吸器内科at 01:09
| 抗凝固療法
医師国家試験:APTT延長
医師国家試験:特発性血小板減少性紫斑病〈ITP〉より続く。
106回医師国家試験の問題紹介を続けさせていただきます。
【設問】
生後6日の男児.頭部の腫瘤を主訴に新生児搬送された.在胎39週2日,3,120gで頭位自然分娩で出生した.仮死はなかった.
出生直後に頭部の腫瘤を認めていた.腫瘤は増大傾向にあり,黄疸と貧血とが出現して次第に増悪してきたため転院した.
意識は清明.身長51.0cm,体重3,080g.両側の頭頂側頭部に径5cmの軟らかい腫瘤を触知する.大泉門の膨隆を認めない.心音と呼吸音とに異常を認めない.腹部は平坦,軟で,肝・脾を触知しない.
血液所見:赤血球233万,Hb 8.7g/dl,Ht 23%,白血球28,400,血小板28万,出血時間正常,PT 11秒(基準10〜14),APTT 70秒(基準対照27〜40),フィブリノゲン322mg/dl(基準130〜380).血液生化学所見:総ビリルビン16.2mg/dl,直接ビリルビン0.1mg/dl,AST 45IU/l,ALT 12IU/l,LD 700IU/l(基準335〜666)
入院時の頭部単純CT冠状断像(略):巨大な頭部皮下血腫。
確定診断に必要な検査項目はどれか.2つ選べ.
a 第VII因子活性
b 第VIII因子活性
c 第IX因子活性
d 第X因子活性
e von Willebrand因子活性
【解説】
腫瘤は皮下血腫です(血腫成分の吸収に伴い、間接ビリルビンやLDHが上昇しているようです)。
APTTの延長がみられますが、PTや出血時間は正常です。
血友病が疑われます。
【正解】b、c
<リンク>
投稿者:血液内科・呼吸器内科at 01:57
| 医師国家試験・専門医試験対策
医師国家試験:特発性血小板減少性紫斑病〈ITP〉
医師国家試験:皮膚の出血斑(紫斑)より続く。
106回医師国家試験の問題紹介を続けさせていただきます。
【設問】
特発性血小板減少性紫斑病〈ITP〉の先行感染として最も多いのはどれか.
a 伝染性紅斑
b 突発性発疹
c 風疹
d 流行性耳下腺炎
e 溶連菌感染症
【解説】
急性特発性血小板減少性紫斑病〈ITP〉は、ウイルス感染症後に多いことが知られていますが、どのウイルスで多いかまで書かれていてない教科書が多いですから、回答に迷った人が多いのではないでしょうか。
麻疹、風疹、水痘の後に、ITP発症がありえます。
【正解】c
(続く)医師国家試験:APTT延長へ
<リンク>
投稿者:血液内科・呼吸器内科at 01:44
| 医師国家試験・専門医試験対策
医師国家試験:皮膚の出血斑(紫斑)
医師国家試験:ビタミンK依存性凝固因子より続く。
106回医師国家試験の問題紹介を続けさせていただきます。
【設問】
68歳の女性。皮膚の出血斑を主訴に来院した。打撲した記憶がないにもかかわらず、数ヶ月前から両側の手背と前腕とに出血斑が見られることが気になっていたという。鼻出血と歯肉出血とを認めない。口腔粘膜に点状出血を認めない。
両側の手背と前腕とに径3〜5cmの紫斑を3個認める。
血液所見:
赤血球468万、Hb13.9g/dl、Ht42%、白血球6,300、血小板20万、PT98%(基準80〜120)、APTT33秒(基準対照32)。
対応として適切なのはどれか。
a. 経過観察
b. 骨髄穿刺
c. 血清免疫電気泳動
d. 血小板凝集能検査
e. 凝固因子活性
【解説】
高齢者の女性で両側の手背と前腕に出血斑がみられていますが、その他の出血症状はみられていません。血小板数、PT、APTTの各検査は正常です(凝固異常を伴っていません)。
老人性紫斑と考えられます。特に、手背と前腕が好発部位です。
老人性紫斑は、高齢者の、前腕、手背などに出現します。境界明瞭で、青紫〜暗紫色です。自然消退しますが、しばしば場所を変えて再出現します。
老人性紫斑は病的なものではなく、放置して良いです。全ての検査結果が正常です。
臨床現場ではしばしば遭遇します。出血斑の画像は確認しておきたいところです。
(続く)医師国家試験:特発性血小板減少性紫斑病〈ITP〉へ
<リンク>
投稿者:血液内科・呼吸器内科at 01:32
| 医師国家試験・専門医試験対策
医師国家試験:ビタミンK依存性凝固因子
医師国家試験:血小板数低下より続く。
106回医師国家試験の問題紹介を続けさせていただきます。
【設問】
ビタミンK依存性の凝固調節因子でないのはどれか。
a 第II因子
b 第VII因子
c プロテインC
d プロテインS
e フィブリノゲン
【解説】
ビタミンK依存性凝固因子は、半減期の短い順番に、第VII因子、第IX因子、第X因子、第II因子です(第VII因子が最も半減期が短いです)。
代表的凝固阻止因子である、アンチトロンビン(AT)、プロテインC(PC)、プロテインS(PS)のうち、PCおよびPSもビタミンK依存性です(参考:先天性血栓性素因と病態/アンチトロンビン・プロテインC&S欠損症)。
a 第II因子(プロトロンビンとも言います)は、ビタミンK依存性凝固因子です。
b 第VII因子は、ビタミンK依存性凝固因子です。ビタミンK依存性凝固因子の中で、第VII因子は最も半減期が短いです。そのために、ビタミンK欠乏症では、まず第VII因子が低下する。PTは第VII因子を反映しますが、APTTは第VII因子を反映しませんので、ビタミンK欠乏症のスクリーニング検査は、APTTではなくPTで行います。
c プロテインCは、ビタミンK依存性凝固阻止因子です。
d プロテインSは、ビタミンK依存性凝固阻止因子です。ワルファリン(ビタミンK拮抗薬)内服中は、誰でもプロテインC、プロテインSともに低下するために、先天性プロテインC欠損症や先天性プロテインS欠損症の診断には注意が必要です。
e フィブリノゲンは、ビタミンK依存性ではありません。
【正答】e
(続く)医師国家試験:皮膚の出血斑(紫斑)へ
<リンク>
投稿者:血液内科・呼吸器内科at 01:02
| 医師国家試験・専門医試験対策
医師国家試験:血小板数低下
医師国家試験:血小板数増加より続く。
106回医師国家試験の問題紹介を続けさせていただきます。
【設問】
45歳の男性。意識障害のため搬入された。
5日前から38℃台の発熱が続いていた。昨日から傾眠状態となり、次第に増悪してきたため家族が救急車を要請した。下痢と血便とはなかったという。
意識レベルはJCSII-30。身長158cm,体重59kg.体温39.0℃.脈拍88/分,整.血圧110/70mmHg.呼吸数28/分.皮膚に出血斑を認める。
尿所見:蛋白2+,潜血2+.
血液所見:赤血球138万,Hb 4.1g/dl,Ht 16%,白血球8,000,網赤血球5%,血小板1.2万,PT 97%(基準80〜120),APTT 32秒(基準対照32).血液生化学所見:総蛋白6.9g/dl,アルブミン3.3g/dl,尿素窒素24mg/dl,クレアチニン0.9mg/dl.
心電図と胸部X線写真とに異常を認めない。
末梢血塗抹May-Giemsa染色標本(略):赤血球破砕像あり。血小板がほとんど見られていない。
治療として適切なのはどれか.
a 血小板輸血
b 抗DIC療法
c 血漿交換療法
d Helicobacter pylori除菌
e 免疫グロブリンの大量投与
【解説】
意識障害、発熱、血小板数減少(ただしPT、APTTは正常)、貧血(赤血球破砕を伴う)が見られています。特に、赤血球破砕像は特徴的で、血栓性微小血管障害症(thrombotic microangiopathy:TMA)と考えられます。
本症例では、腎機能障害はみられていません(HUSではありません)。
PT、APTTは正常です。
おそらくDICではないとの出題者の意図であると思われますが、本当はPT、APTTのみではDIC合併を否定しきれあせん。
実臨床では、DIC合併の有無のチェックのためにはFDP、Dダイマー、TATなどの測定が不可欠です(参考:DIC図解シリーズ )。
診断は、血栓性血小板減少性紫斑病(thrombotic thrombocytopenic purpura:TTP)です。
a 血小板輸血は、TTPに対して禁忌です。
b DICではないので、DICの治療は行ってはいけません。
c 血漿交換療法は、TTPに対するfirst choiceです。
d Helicobacter pylori除菌療法は、特発性血小板減少性紫斑病(ITP)に対して行われることがあります。
e 免疫グロブリンの大量投与は、ITPに対する摘脾術に先立ち、一過性に血小板数を上昇させる目的で行われることがあります。
TTPでは、微小血管内皮障害、および血小板活性化が原因となって、微小な血小板血栓が多発し、血小板数低下に伴う出血傾向とともに、動揺する精神症状をきたします。
多発した微小血栓間を通過するため、赤血球破砕し溶血性貧血の所見もきたします。
<TTPの五主徴>
1. 血小板数減少
2. 溶血性貧血(赤血球破砕像)
3. 動揺する精神症状
4. 腎障害
5. 発熱
TTPの発症機序が近年明らかになりました。
ADAMTS13(von Willebrand因子(vWF)切断酵素(vWF-CP)とも言います)に対する自己抗体が出現することにより、この酵素活性が著減します。
その結果、unusually large vWFが出現し、血小板凝集が進行します。
溶血性尿毒症症候群(HUS)では、この自己抗体の出現はありません。
【正解】c
(続く)医師国家試験:ビタミンK依存性凝固因子へ
<リンク>
投稿者:血液内科・呼吸器内科at 01:38
| 医師国家試験・専門医試験対策
医師国家試験:血小板数増加
先日、106回医師国家試験が行われました。
今回から、血栓止血領域の問題の一部を、何回かに分けて紹介させていただきます。
【設問】
70歳の男性。定期健康診断で検査値の異常を指摘されたため来院した。
1年前に脳梗塞の既往がある。
心音と呼吸音とに異常を認めない。肝・脾を触知しない。
血液所見:
赤血球468万,Hb 13.9g/dl,Ht 42%,白血球12,300(桿状核好中球30%,分葉核好中球45%,好酸球1%,好塩基球1%,単球6%,リンパ球17%),血小板250万.骨髄検査では線維化を認めず。染色体は正常核型である。
末梢血塗抹May-Giemsa染色標本(略):血小板の多い血液像。
骨髄生検のH-E染色標本(略):成熟した巨核球の増加した骨髄像。
診断として最も考えられるのはどれか。
a 骨髄線維症
b 慢性骨髄性白血病
c 骨髄異形成症候群
d 真性赤血球増加性
e 本態性血小板血症
【解説】
何と言っても、血小板数の著増が特徴的である。
血小板数の著増&白血球数の軽度上昇から骨髄増殖性疾患を疑います(反応性血小板増加症では血小板数が100万/μL以上になることは稀です)。
Hbの上昇はなく真性赤血球増加症は否定されます。
染色体異常(転座t(9:22))もなく、CMLも否定されます。
骨髄検査では線維化を認めず、慢性特発性骨髄線維症でもありません。
末梢血液像では血小板数の増加が、骨髄病理では成熟した巨核球の増加が確認されています。
本態性血小板血症(ET)と考えられます。
本態性血小板血症では血小板数が著増して血栓症をきたしやすいですが、一方で血小板の機能が低下しているために、出血もきたしやすいのが特徴です。
抗血栓療法(低用量アスピリン)で加療することが多いです。必要に応じて、化学療法(ヒドロキシウレアなど)を行います。
約半数例で、JAK2遺伝子変異を伴います(参考:JAK2遺伝子変異と血栓症)。
【正答】e
(続く)医師国家試験:血小板数低下へ
<リンク>
投稿者:血液内科・呼吸器内科at 01:06
| 医師国家試験・専門医試験対策
PT・APTT・フィブリノゲン試薬の使用状況(シェア)
日本医師会 臨床検査精度管理調査 試薬利用状況(凝固)からの情報です。
PT、APTT、フィブリノゲン(Fbg)のシェアです。
1)PT
2)APTT
3)フィブリノゲン(Fbg)
投稿者:血液内科・呼吸器内科at 01:21
| 医学全般
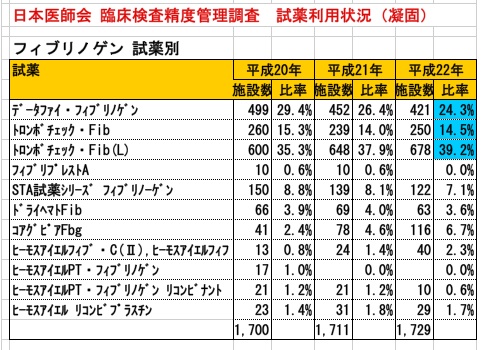
フィブリノゲン(Fbg)試薬の使用状況(シェア)
日本医師会 臨床検査精度管理調査 試薬利用状況(凝固)からの情報です。
日本でのフィブリノゲン試薬の使用状況がわかります。
金沢大学附属病院の検査部では、トロンボチェック・Fib(L)を使用しています。
投稿者:血液内科・呼吸器内科at 01:09
| 医学全般
多発性骨髄腫とレブラミド
Multiple Myeloma Seminar in Kanazawa
日時:2012年3月16日(金)19:00〜21:00
会場:ANAクラウンプラザホテル金沢 2F『セラヴィ』
プログラム
19:00-19:15 学術情報
「レブラミドの最新情報」 セルジーン(株)医学本部 学術担当
19:15-19:45
一般演題
金沢医科大学 血液免疫内科学 教授 岡崎俊朗 先生
石川県立中央病院 血液内科 診療部長 澤�愛子 先生
『北陸多施設共同後方視的多研究について(仮)』
金沢医科大学 血液免疫内科学 准教授 福島俊洋 先生
『レブラミドに関する症例提示(仮)』
19:45-20:45
特別講演
金沢大学医薬保健研究域医学系 細胞移植学 教授 中尾眞二
『多発性骨髄腫—新たな治療戦略の展開—』
新潟県立がんセンター新潟病院 張 高明 先生
主催:セルジーン株式会社
【リンク】
投稿者:血液内科・呼吸器内科at 01:46
| 研究会・セミナー案内
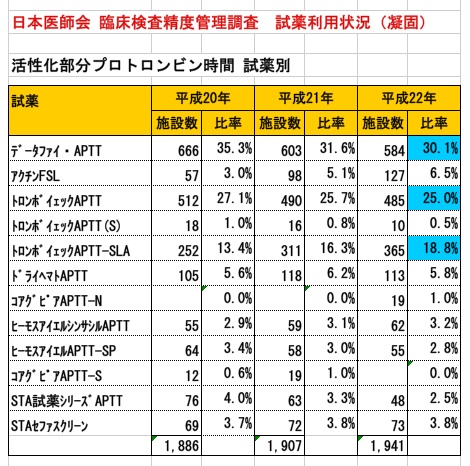
活性化部分トロンボプラスチン時間(APTT)試薬(シェア)
日本医師会 臨床検査精度管理調査 試薬利用状況(凝固)からの情報です。
金沢大学では、現在トロンボイェックAPTT-SLAを使用しています。
<リンク>
投稿者:血液内科・呼吸器内科at 01:58
| 医学全般
プロトロンビン時間(PT)試薬の使用状況(シェア)
日本医師会 臨床検査精度管理調査 試薬利用状況(凝固)からの情報です。
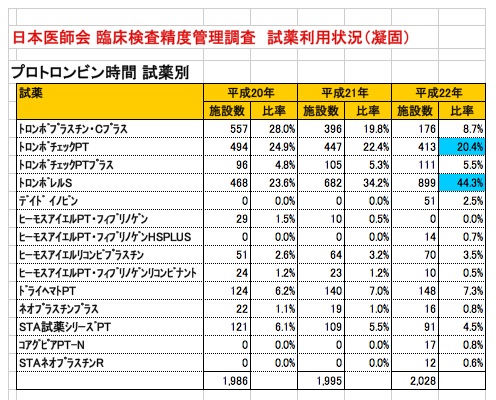
トロンボプラスチン・Cプラスは、販売中止となっているため、次回から更に比率低下の見込みです。
金沢大学では、現在トロンボレルSを使用しています。
<リンク>
投稿者:血液内科・呼吸器内科at 01:21
| 医学全般
DICの治療戦略(インデックス)
DICの治療:固形癌より続く
DICの治療戦略(13)インデックス
投稿者:血液内科・呼吸器内科at 01:31
| DIC
DICの治療:固形癌
DICの治療:敗血症より続く
DICの治療(基礎疾患別)(12)固形癌
固形癌に合併したDICの治療
DICを合併した固形癌においては多くの場合、全身転移をともなった進行癌症例であることが多いです(参考:
悪性腫瘍(癌)とDIC)。
換言すれば、早期癌でDICを合併することは極めて例外的です。
基礎疾患に対して化学療法を行うことで腫瘍量が低下する場合にはDICのコントロールは容易ですが、腫瘍量の低下が期待できない場合のDIC治療は困難です。
DIC治療を行っても、予後改善効果がほとんど期待できない場合は、DIC治療を行わないのも一つの考え方です。
その場合であっても、出血予防のための、PCやFFPの輸注は意味のある場合があります。
一方、進行癌であってもDICの治療を行うことで、十分な予後改善が期待できる場合も少なくないです。
この場合は、DIC治療の意義は高いです。
著者らは、進行癌でDICを合併していたにもかかわらず、DICの治療により、1年以上の生命予後が可能となった症例を蓄積しています。
抗凝固療法としては、
ダナパロイド1,250単位×2回/日(腎不全例や低体重例では1回/日に減量)または
低分子ヘパリン75単位/kg/24時間の投与を行います。
慢性DICの経過をとっていて、患者を24時間持続点滴で拘束したくない場合には、ダナパロイドによる加療の方が有用です。
一部の固形癌(前立腺癌、悪性黒色腫、大腸癌や肺癌の一部)に合併したDICでは線溶活性化が著しく、重症の出血症状を伴った線溶亢進型DICの病型となることがあります(参考:
悪性腫瘍(癌)とDIC)。
この場合には、
メシル酸ナファモスタット(商品名:
フサン)、または
ヘパリン類&
トラネキサム酸併用療法が、出血症状に対して著効します(その結果、PCやFFP使用量を少なくすることが可能です)。
(続く)
DICの治療戦略(インデックス)へ
【リンク】
投稿者:血液内科・呼吸器内科at 01:22
| DIC
DICの治療:敗血症
DICの治療:急性前骨髄球性白血病(APL) より続く
DICの治療(基礎疾患別)(11)敗血症
敗血症に合併したDICの治療
感受性を有した抗生剤投与が最重要です。
抗凝固療法としては、AT濃縮製剤を、1日1,500単位、3〜5日間投与します。
敗血症に合併したDICにおいては多くの例で、
AT活性が低下するため、AT濃縮製剤が必要となることが多いです。
日本で認可されているAT濃縮製剤の使用量は大変少なく、充分な凝固活性を期待するためには、
ダナパロイド1,250単位×2回/日(腎不全例や低体重例では1回/日に減量)または
低分子ヘパリン(75単位/kg/24時間)を併用します(参考:
ヘパリン類)。
未分画ヘパリンはかえって予後を悪くする可能性が指摘されており、推奨されません。
遺伝子組換え
トロンボモジュリン製剤(rTM)(商品名:
リコモジュリン)は、敗血症に合併したDICに対しても有効であり、今後も使用頻度が増加する可能性が高いです。
前述のように、AT濃縮製剤とrTMの併用が認められるような医療環境になって欲しいところです。
トランサミンは臓器障害を悪化させるため、絶対禁忌です。
敗血症に合併したDICではしばしば肝不全を合併するため、
PTの著明な延長やフィブリノゲンの著明な低下がみられることがあり、この場合にはFFPを投与します。
食事摂取ができない状態で長期間の抗生剤が投与されることに伴って、
ビタミンK欠乏症を併発する可能性があるため、ビタミンK 10mg/日程度の予防投与(点滴)を行っておく方が無難です。
(続く)
DICの治療:固形癌へ
【リンク】
投稿者:血液内科・呼吸器内科at 01:48
| DIC
DICの治療:急性前骨髄球性白血病(APL)
DICの治療:急性白血病(APL以外)より続く
DICの治療(基礎疾患別)(10)急性前骨髄球性白血病(APL)
APLに合併したDICの治療
APLは、典型的な
線溶亢進型DICを発症します。
DICに対して適切な治療が行われませんと、脳出血を含め、致命的な出血をきたすことがあります。
急性白血病の中でも、APLに合併したDICの特殊性として、
ATRAによる治療が行われることがあります。
ATRAは、APLの分化誘導としても有効であるが、APLに合併したDICに対してもしばしば著効します。
しかも、APLの分化誘導に成功するよりも遥かに早く、DICの改善傾向をもたらすことも多いです(1〜2日くらいのこともあります)。
これに伴い、出血症状も速やかに消退することが多いです。
APLにおいてDICを発症する原因は、他の白血病と同様に、白血病細胞中に含有されているTFによる外因系凝固機序の活性化と考えられています。
さらに、APLにおいて線溶亢進型DICを合併する理由は、APL細胞に存在する
アネキシンIIの果たす役割が大きいと考えられています。
Menell, et al: Annexin II and bleeding in acute promyelocytic leukemia. N Engl J Med 340: 994-1004, 1999.
アネキシンIIは、組織プラスミノゲンアクチベーター(tissue plasminogen activator:t-PA)と、プラスミノゲンの両線溶因子と結合することが可能ですが、このことで、t-PAによるプラスミノゲンの活性化能が飛躍的に高まることが知られています。
大変興味深いことに、
APLに対してATRAを投与しますと、APL細胞中のTFが抑制されることに加えて、上記のアネキシンIIの発現も抑制されます。
このため凝固活性化と線溶活性化に同時に抑制がかかり、APLのDICは速やかに改善するものと考えられます。
なお、ATRAによるアネキシンII発現の抑制は相当に強力であるらしく、APLの著しい線溶活性化の性格は速やかに消失します。
前述のように、APLに対してATRAを投与している場合に、
トラネキサム酸を投与すると全身性血栓症や突然死の報告がみられます。
APLに対してATRAを投与する場合には、トラネキサム酸は絶対禁忌です。
(続く)
DICの治療:敗血症へ
【リンク】
投稿者:血液内科・呼吸器内科at 01:13
| DIC
DICの治療:急性白血病(APL以外)
DICの治療:免疫グロブリン製剤より続く
DICの治療(基礎疾患別)(9)急性白血病(APL以外)
急性白血病(APL以外)に合併したDICの治療
急性白血病に対して、適切な化学療法を行うことが最重要です。
抗凝固療法としては、歴史的には、
未分画ヘパリンが頻用されてきましたが、出血の副作用の問題があるため、近年はあまり使用されません。
出血の副作用が少ない
低分子ヘパリンや
ダナパロイドの方がヘパリン類の中では使用される機会が多くなっています。
ただし、これらのヘパリン類は、未分画ヘパリンよりも出血の副作用が少ないですが、全くないという訳ではありません。
メシル酸ナファモスタット(
フサン)やメシル酸ガベキサートは、出血の副作用がほとんどないため、白血病が基礎疾患のように出血しやすいDICには良い適応となります。
特に、メシル酸ナファモスタットは、現在の臨床用量で線溶抑制効果も強力であり、
線溶亢進型〜線溶均衡型DICに対して有効な治療薬です。
管理人らは、メシル酸ナファモスタットは急性白血病に合併したDICに対して最も相性が良い薬剤の一つと考えています。
急性白血病に合併したDICにおいては
AT活性が低下することが少なく、AT濃縮製剤の使用頻度は少ないです。
rTM(
リコモジュリン)は、造血器悪性腫瘍に合併したDICに対しても未分画ヘパリン以上に有効であり4)、今後、使用頻度が急増する可能性が高いです。
血液内科領域では、移植関連の肝中心静脈閉塞症(veno-occlusive disease:VOD)や、血栓性微小血管障害症(thrombotic microangiopathy, TMA)に対しての期待も大きいようですが、現時点ではエビデンスはなく保険認可もされていません。
急性白血病では、DICコントロールを行っても血小板数の回復は期待できないために、しばしばPCの輸注が必要となります(
DICの補充療法)。
線溶活性化が著しいDICの極期においては、血小板数から想定される以上に出血傾向が高度である点に留意が必要です。
フィブリノゲンが著明に低下したり、プロトロンビン時間(
PT)が著明に延長した症例に対しては、FFPによる凝固因子の補充を行います。
(続く)
DICの治療:急性前骨髄球性白血病(APL)へ
【リンク】
投稿者:血液内科・呼吸器内科at 01:25
| DIC
DICの治療:免疫グロブリン製剤
DICの治療:抗線溶療法 より続く
DICの治療(治療法別)(8)免疫グロブリン製剤
5) 免疫グロブリン (DIC治療の番外編)
特に、重症感染症に合併したDICにおいてはサイトカインが重要な役割を演じています(
敗血症に合併したDICの発症機序)。
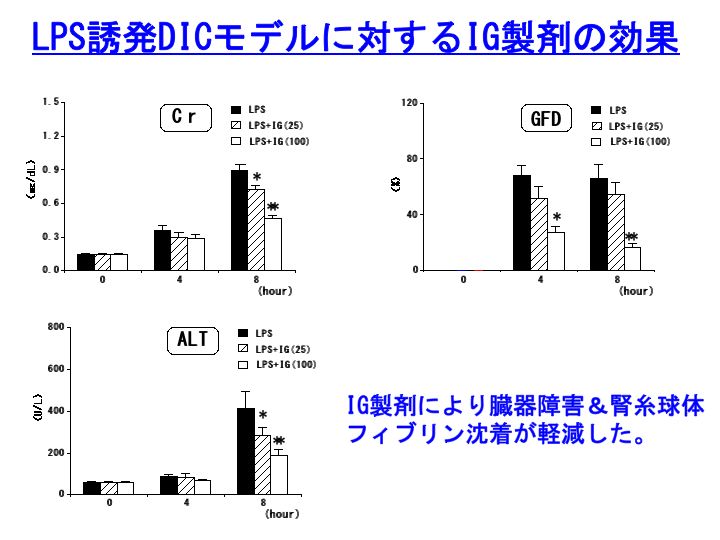
我々の動物DICモデルを用いた検討では、LPS誘発DICモデルに対して免疫グロブリンを投与しますと、TNFやIL-6と言った炎症性サイトカインが抑制され、DIC病態が有意に軽快しました(上図)。
Immunoglobulin preparations attenuate organ dysfunction and hemostatic abnormality by suppressing the production of cytokines in LPS-induced DIC in rats. Crit Care Med 34: 2421-2425, 2006.
免疫グロブリンは、臨床でのDIC治療薬としても威力を発揮する可能性が高いです。
(続く)
DICの治療:急性白血病(APL以外)へ
【リンク】
投稿者:血液内科・呼吸器内科at 01:06
| DIC
DICの治療:抗線溶療法
DICの治療:補充療法より続く
DICの治療(治療法別)(7)抗線溶療法
4) 抗線溶療法
DICにおける線溶活性化は、微小血栓を溶解しようとする生体の防御反応の側面もあり、トラネキサム酸(商品名:
トランサミン)などの抗線溶療法は原則禁忌です。
特に、敗血症に合併したDICでは絶対禁忌です。
人道的に敗血症性DICの臨床例に対してトラネキサム酸を投与してはいけませんが、ラットのLPS誘発DICモデル(敗血症性DICのモデル)に対してトラネキサム酸を投与するとほとんど全てのラットが臓器不全を伴って死亡してしまいます(参考:
ラットDICモデルに対する抗線溶療法)。
また、
急性前骨髄球性白血病(APL)症例において、all-trans retinoic acid(ATRA)による分化誘導療法を行っている場合も、トラネキサム酸を投与すると全身性血栓症を併発して死亡したという報告が多数見られるため、絶対禁忌です。
APLに対して
ATRAを投与しますと、APLの本来の
線溶亢進型DICの性格が変化して、線溶抑制型DICの病態に近付くものと考えられます。
ただし、線溶亢進型DICの著しい出血例に対して、ヘパリン類併用下に
トラネキサム酸を投与しますと出血に対してしばしば著効することがありますが、使用方法を間違うと全身性血栓症をきたすために、必ず専門家にコンサルトの上で行う必要があります。
また、線溶亢進型以外のDICに対しては、トラネキサム酸は禁忌であるため
線溶亢進型DICの診断は万全を期する必要があります。
(続く)
DICの治療:免疫グロブリン製剤へ
【リンク】
投稿者:血液内科・呼吸器内科at 01:00
| DIC
DICの治療:補充療法
DICの治療:遺伝子組換えトロンボモジュリン製剤より続く
DICの治療(治療法別)(6)補充療法
3) 補充療法
血小板や凝固因子の著しい低下(消費性凝固障害)のため出血がみられる場合には、補充療法を行います。
血小板の補充目的としては
濃厚血小板(platelet concentrates:PC)、凝固因子の補充目的としては
新鮮凍結血漿(fresh frozen plasma:FFP)を用います。
通常、PCは血小板数2万/μL程度以上に維持されることを目安に輸注します。
PC 10〜20単位/1回を、必要があれば経日的に繰り返します。
FFP は、フィブリノゲン100mg/dl未満またはPT比1.7以上になるような症例では必要になることが多いです。
FFP 400〜500mL程度/1回を、必要があれば経日的に繰り返します。
(続く)
DICの治療:抗線溶療法へ
【リンク】
投稿者:血液内科・呼吸器内科at 01:03
| DIC
DICの治療:遺伝子組換えトロンボモジュリン製剤
DICの治療:合成プロテアーゼインヒビターより続く
DICの治療(治療法別)(5)遺伝子組換えトロンボモジュリン製剤
2) 抗凝固療法
c. 遺伝子組換えトロンボモジュリン製剤
遺伝子組換えトロンボモジュリン製剤(recombinant thrombomodulin:rTM)(商品名:
リコモジュリン)は、日本で使用されるDIC治療薬の中で、最も質の高い臨床試験において有用性が証明されており、今後大変期待されている薬剤の一つです。
Saito H, et al: Efficacy and safety of recombinant human soluble thrombomodulin (ART-123) in disseminated intravascular coagulation: results of a phase III, randomaized, double-blind clinical trial. J Thromb Haemost 5: 31-41, 2007.
出血の副作用が少ないにもかかわらず、
ヘパリン類と同等以上の抗凝固活性が期待できます。
臨床で使用されることになる本薬の用量では、トロンビンが存在する状況でのみ抗凝固活性を発揮する(DICが改善してトロンビンがなくなると抗凝固活性を発揮しない)ことが、出血の副作用が少ない理由の一つではないかと考えられます。
なお、本薬には抗炎症効果が報告されています。
Abeyama K, et al: The N-terminal domain of thrombomodulin sequesters high-mobility group-B1 protein, a novel antiinflammatory mechanism. J Clin Invest 115: 1267-1274, 2005.
炎症性疾患に合併したDICに対して、抗凝固、抗炎症の両面から期待されています(炎症と凝固のクロストークの遮断)。
可能であれば、AT濃縮製剤と併用投与したいところですが、保険上の扱いがどうなるか、この記事アップ時点では不明です。
(続く)
DICの治療:補充療法へ
【リンク】
投稿者:血液内科・呼吸器内科at 01:35
| DIC
血液疾患検査 expert seminar のご案内
血液疾患検査 expert seminar
日時:平成24年2月11日(土) 17:30 〜
場所:石川県地場産業振興センター新館「第12研修室」(金沢市鞍月2-1)
総合司会 金沢医科大学血液免疫内科学 教授 岡崎 俊朗 先生
【講演1】17:30 – 18:00
座長 金沢大学医薬保健研究域医学系 細胞移植学 中尾 眞二
『血液疾患における臨床検査の進歩』
演者 東京大学大学院医学系研究科 臨床病態検査医学教授 矢冨裕 先生
【講演2】18:00 – 18:45
座長 金沢大学医薬保健研究域医学系 血液情報統御学 教授
同 附属病院 腎臓内科長 和田 隆志 先生
『造血器腫瘍遺伝子検査の実際−当院の知見を含めて−』
演者 東京大学医学部附属病院 検査部 技師長 横田 浩充 先生
【講演3】18:45 – 19:30
座長 金沢医科大学 血液免疫内科学 臨床准教授 正木 康史 先生
『血液疾患におけるフローサイトメトリー』
演者 京都大学医学部附属病院 検査部 副技師長 大森 勝之 先生
主催:中外製薬株式会社
【リンク】
投稿者:血液内科・呼吸器内科at 01:11
| 研究会・セミナー案内
DICの治療:合成プロテアーゼインヒビター
DICの治療:抗凝固療法/ヘパリン/アンチトロンビン より続く
DICの治療(治療法別)(4)合成プロテアーゼインヒビター
2) 抗凝固療法
b. 合成プロテアーゼインヒビター
合成プロテアーゼインヒビター(serine protease inhibitor:SPI)は、AT非依存性に抗トロンビン活性を発揮します。
代表的薬剤は、
メシル酸ナファモスタット(商品名:
フサンなど)および、メシル酸ガベキサート(商品名:FOYなど)です。
出血の副作用は皆無に近いため、出血の副作用のためにヘパリン類の使用が困難な場合には良い適応となります。
また、両薬剤は膵炎治療薬でもあり、DICのみならず膵炎をも合併している時にも良い適応となります。
メシル酸ナファモスタットは、臨床使用量(1.44〜4.8mg/kg/日、持続点滴静注:標準的体重の人では150〜200mg/24時間)で、抗凝固活性のみならず抗線溶活性も強力であり、
線溶亢進型DICに対して有効です。
メシル酸ガベキサートは臨床使用量(20〜39mg/kg/日、持続点滴静注:標準的体重の人では1,500〜2,000 mg/24時間)では抗線溶活性は強くありません。
なお、メシル酸ナファモスタットの高カリウム血症の副作用には注意が必要です。
両薬剤ともに静脈炎の副作用があり、中心静脈からの投与が原則です。
(続く)
DICの治療:遺伝子組換えトロンボモジュリン製剤へ
【リンク】
投稿者:血液内科・呼吸器内科at 01:15
| DIC
金沢大学第三内科 同門会総会・開講記念会のご案内(H24年)
金沢大学第三内科 同門会会員各位
金沢大学第三内科 関係各位
<第三内科同門会のご案内>
本年の同門会は、
平成24年6月17日(日)13時〜(於:金沢エクセルホテル東急)
になりました。
詳細は後日に案内させていただきますが、皆様の手帳に予定を書き込んでいただければと思います。
今後ともどうぞよろしくお願いいたします。
【リンク】
投稿者:血液内科・呼吸器内科at 01:28
| その他
へパリンカルシウム:在宅自己注射の保険適用認可
投稿者:血液内科・呼吸器内科at 01:30
| 血栓性疾患
DICの治療:抗凝固療法/ヘパリン/アンチトロンビン
DICの治療(治療法別):基礎疾患の治療より続く
DICの治療(治療法別)(3)抗凝固療法(ヘパリン&アンチトロンビン)
2) 抗凝固療法
日本でDICに対して使用可能な抗凝固療法(参考:
治療の種類)としてはいくつかの薬剤が知られていますが、DICの病態に応じて適切な薬剤を選択します。
a. ヘパリン類&アンチトロンビン濃縮製剤
現在の日本においてDICに対して使用可能な
ヘパリン類としては、ダナパロイドナトリウム(商品名:
オルガラン)、低分子ヘパリン(商品名:
フラグミンなど)、未分画ヘパリン(標準ヘパリン)があります。
これらのヘパリン類は、いずれも
アンチトロンビン(AT)活性を促進させることによって、抗凝固活性を発揮する点で共通していますが、抗Xa/トロンビン(IIa)活性比や、血中半減期には相当な差違がみられます(参考:ヘパリン類)。
これらのヘパリン類の特徴を見極めながら、使い分ける必要があります。
ダナパロイドナトリウムは半減期が長いために、1日2回の静注(1,250単位を、1日2回12時間毎に静注)であっても効果が持続する点が魅力です。
この点、
慢性DICに対しては最も良い適応となります(患者を24時間持続点滴で拘束する必要がありません)。
ただし、万一出血の副作用がみられた場合には半減期の長いことがデメリットになる場合があります。
また、腎代謝のため、腎機能障害のある症例や低体重の症例では減量して使用すべきです(他のヘパリン類にも当てはまる)。
ヘパリン類は、AT活性が低下した場合は充分な効果が期待できないため、AT濃縮製剤(商品名:アンスロビンP、ノイアート、ノンスロン)を併用します。
保険適応は、AT活性70%以下の症例でAT濃縮製剤を使用することが可能であり、1,500単位/日で3〜5日間使用されます。
ただし、この保険上の使用方法には医学的根拠はなく、より大量に使用できれば理想的です。
未分画ヘパリンは、ダナパロイドナトリウムや低分子ヘパリンと比較して医学的に優れている点はあまりありません。
未分画ヘパリン24時間持続点滴は、現在ほとんど使用されなくなってきています(未分画ヘパリンは安価である点のみがメリットです)。
しかし、
へパリンカルシウムの在宅自己注射(皮下注)の保険適用認可というビッグニュースがあります。
今後、慢性DIC(腹部大動脈瘤など)に対して、
へパリンカルシウムの在宅自己注射(皮下注)は普及していくようになるのではないかと思います。
(続く)
DICの治療:合成プロテアーゼインヒビターへ
【リンク】
投稿者:血液内科・呼吸器内科at 01:53
| DIC
DICの治療(治療法別):基礎疾患の治療
DICの治療(治療法別):種類より続く
DICの治療(治療法別)(2)基礎疾患の治療
1)基礎疾患の治療(参考:
DICの基礎疾患)
全てのDICには必ず基礎疾患が存在します。
どのような症例においても、基礎疾患の治療は最重要です。
急性白血病や進行癌に対する化学療法、敗血症に対する感受性のある抗生剤治療などがこれに相当します。
なお、
悪性腫瘍(造血器を含む)に対して化学療法を行いますと、腫瘍細胞の崩壊に伴って組織因子(tissue factor: TF)が大量に血中に流入するため、DICが一時的にかえって悪化することが少なくありません。
ただし、それを理由に基礎疾患の治療を躊躇してはいけません。
(続く)
DICの治療:抗凝固療法/ヘパリン/アンチトロンビンへ
【リンク】
投稿者:血液内科・呼吸器内科at 01:45
| DIC
DICの治療(治療法別):種類
DICの治療(治療法別)(1)種類
1)基礎疾患の治療:最も重要(参考:
DICの基礎疾患)
2)抗凝固療法:下記より選択
1.
ヘパリン類:ダナパロイド(
オルガラン)、低分子ヘパリン(
フラグミンなど)、未分画ヘパリン
2.
アンチトロンビン濃縮製剤(アンスロビンP、ノイアート、ノンスロン)
3. 遺伝子組換え
トロンボモジュリン製剤(
リコモジュリン)
4. 合成プロテアーゼ阻害薬:
メシル酸ナファモスタット(
FUTなど)、メシル酸ガベキサート(FOYなど)
3)補充療法
1. 濃厚血小板(PC):血小板の補充
2. 新鮮凍結血漿(FFP):凝固因子の補充
4)抗線溶療法:
・原則禁忌(線溶抑制型DICでは絶対禁忌)
・ただし、重症の(致命的な)出血症状をきたした線溶亢進型DICに対しては、ヘパリン類との併用のもとにトラネキサム酸(
トランサミン)の投与が著効することがあります。
このあと、少しずつシリーズで記事にしていきたいと思います。
(続く)
DICの治療(治療法別):基礎疾患の治療へ
【リンク】
投稿者:血液内科・呼吸器内科at 01:27
| DIC